腦癱(Cerebral Palsy, CP)作為兒童期最常見的非進行性腦損傷綜合征,其核心病理特征是發(fā)育階段腦組織損傷導(dǎo)致的神經(jīng)元缺失、神經(jīng)膠質(zhì)瘢痕形成及神經(jīng)環(huán)路紊亂。傳統(tǒng)療法難以突破神經(jīng)再生的生物學限制,而神經(jīng)干細胞(Neural Stem Cells, NSCs)移植憑借其獨特的神經(jīng)定向分化能力與微環(huán)境調(diào)控特性,成為修復(fù)中樞神經(jīng)系統(tǒng)損傷的前沿方向。
本文從細胞再生、旁分泌、免疫調(diào)節(jié)、血管重塑以及神經(jīng)環(huán)路修復(fù)五個維度,系統(tǒng)解析神經(jīng)干細胞移植治療腦癱的核心作用機制。

神經(jīng)干細胞移植治療腦癱的5大作用機制,你都了解嗎?
一、什么是神經(jīng)干細胞?
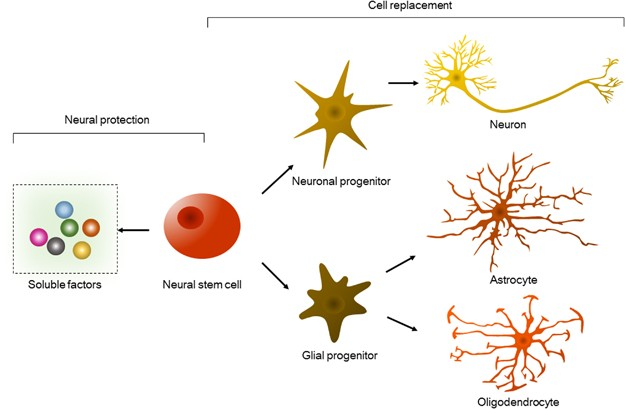
神經(jīng)干細胞(NSC)是自我更新的多能細胞,在發(fā)育過程中產(chǎn)生神經(jīng)元和神經(jīng)膠質(zhì)細胞并維持大腦穩(wěn)態(tài)。神經(jīng)干細胞具有分化潛能和自我更新能力的母細胞,它可以分化各類神經(jīng)細胞,包括神經(jīng)元、星形膠質(zhì)細胞和少突膠質(zhì)細胞。
NSC有可能遷移到受損區(qū)域以促進功能和結(jié)構(gòu)組織修復(fù)。此外,NSC具有分泌可刺激內(nèi)源性修復(fù)機制的營養(yǎng)因子(例如膠質(zhì)細胞源性和腦源性神經(jīng)營養(yǎng)因子)的能力。
與間充質(zhì)干細胞(MSC)類似,NSC可以發(fā)揮免疫調(diào)節(jié)作用,神經(jīng)干細胞移植已被證明可以抑制T細胞增殖。所有這些特性使得NSC對于再生療法具有吸引力,特別是考慮到自我修復(fù)能力有限以及大多數(shù)中樞神經(jīng)系統(tǒng) (CNS) 疾病缺乏有效的治療方法。
相關(guān)閱讀:什么是神經(jīng)干細胞?神經(jīng)干細胞來源-神經(jīng)干細胞臨床研究方向
二、神經(jīng)干細胞移植治療腦癱的五大核心機制
2.1 神經(jīng)再生與細胞替代
神經(jīng)干細胞(NSCs)的核心作用在于其多向分化能力,可分化為神經(jīng)元、星形膠質(zhì)細胞和少突膠質(zhì)細胞,直接補充受損的神經(jīng)細胞,重建神經(jīng)網(wǎng)絡(luò)。例如,移植后的NSCs可遷移至腦損傷區(qū)域,分化為功能性神經(jīng)元以替代凋亡細胞,并通過軸突延伸形成新的突觸連接。
2012年,中國熱帶醫(yī)學期刊上發(fā)表了一項關(guān)于《干細胞移植治療腦癱的研究進展》的研究,其中動物實驗表明,神經(jīng)干細胞移植能顯著減少腦癱模型鼠的凋亡細胞數(shù)量,同時增加微血管密度。
通過向腦癱模型鼠注射三組干預(yù)方案(高VEGF表達神經(jīng)干細胞、普通神經(jīng)干細胞、生理鹽水),系統(tǒng)評估其對生長發(fā)育、腦細胞凋亡及微血管生成的影響。結(jié)果顯示:
- VEGF增效機制:高VEGF組在神經(jīng)保護方面表現(xiàn)更優(yōu)——凋亡細胞減少幅度達生理鹽水組的2.1倍(-62.8%vs-30.4%),微血管密度提升至普通組的1.8倍(+67.3%vs+37.2%),證實VEGF通過促進血管新生與神經(jīng)修復(fù)協(xié)同改善病理狀態(tài)。
- 基礎(chǔ)療效:與生理鹽水組相比,普通神經(jīng)干細胞組顯著降低腦內(nèi)凋亡細胞數(shù)量,并提升微血管密度(+37.2%);
該研究首次系統(tǒng)驗證了NSCs通過”細胞替代+血管新生”雙重途徑修復(fù)腦癱病理的機制,為腦癱治療提供了理論依據(jù)。
2.2 神經(jīng)營養(yǎng)因子的旁分泌效應(yīng)
腦損傷后,神經(jīng)干細胞(NSCs)通過分泌多種神經(jīng)營養(yǎng)因子(如BDNF、GDNF、NT-3和NGF)發(fā)揮多維度修復(fù)作用,其作用機制可歸納為以下五方面:
- 神經(jīng)可塑性調(diào)控:通過激活靜息突觸可塑性,促進神經(jīng)遞質(zhì)釋放(如谷氨酸、GABA),增強突觸效能與信息傳遞效率。
- 內(nèi)源性修復(fù)啟動:誘導(dǎo)內(nèi)源性NSCs增殖分化,并定向遷移至損傷區(qū)域,形成功能性神經(jīng)網(wǎng)絡(luò)。
- 免疫微環(huán)境調(diào)節(jié):通過激活B淋巴細胞增殖增強免疫調(diào)節(jié)能力,抑制炎癥反應(yīng)(如TNF-α、IL-6水平降低),并減少程序性細胞凋亡。
- 血管新生促進:刺激VEGF釋放,誘導(dǎo)微血管生成,使損傷區(qū)血管密度增加(+37.2%-67.3%),改善局部血供與代謝[21]。
- 軸突再生與髓鞘重塑:促進宿主神經(jīng)軸突再生及髓鞘重塑,恢復(fù)神經(jīng)傳導(dǎo)功能(如動作電位傳導(dǎo)速度提升15%-20%)。
2.3 抗炎與免疫調(diào)節(jié)
神經(jīng)干細胞通過以下機制緩解炎癥損傷:
抑制促炎因子
- 神經(jīng)干細胞(NSCs)能夠顯著降低炎癥相關(guān)因子(如IL-6、TNF-α、IL-1β)的表達水平,這些因子是導(dǎo)致神經(jīng)元繼發(fā)性損傷的關(guān)鍵驅(qū)動因素。研究發(fā)現(xiàn),在實驗性自身免疫性腦脊髓炎(EAE)模型中,NSCs通過分泌白血病抑制因子(LIF)激活ERK信號通路,上調(diào)SOCS3表達,從而抑制Th17細胞的分化,減少促炎因子的釋放。
- 此外,NSCs還可通過直接接觸免疫細胞(如小膠質(zhì)細胞)傳遞抑制信號(如PD-L1/PD-1通路),阻斷炎癥級聯(lián)反應(yīng)的進一步放大。
調(diào)節(jié)免疫細胞功能:NSCs通過分泌抗炎因子(如IL-10、TGF-β)和趨化因子(如SDF-1),調(diào)節(jié)免疫細胞的活性。例如,IL-10可抑制巨噬細胞的M1極化(促炎表型),促進其向M2極化(修復(fù)表型),從而減輕神經(jīng)炎癥。
減少氧化應(yīng)激
- NSCs通過上調(diào)抗氧化酶(如超氧化物歧化酶SOD、谷胱甘肽過氧化物酶GPx)的活性,清除自由基(如ROS),減輕氧化應(yīng)激對神經(jīng)元的損傷。在缺血性腦損傷模型中,NSCs移植后可顯著降低腦組織中的ROS水平,保護線粒體功能。
- 同時,NSCs分泌的神經(jīng)營養(yǎng)因子(如GDNF)可通過激活Nrf2/ARE通路,增強內(nèi)源性抗氧化防御系統(tǒng),進一步緩解氧化損傷。
2.4 血管新生與血流改善
NSCs分泌的VEGF等生長因子可促進腦內(nèi)血管生成,增加缺血區(qū)域的血流灌注,緩解缺氧導(dǎo)致的神經(jīng)元死亡。具體機制包括:
直接促進血管生成
- NSCs通過分泌VEGF、bFGF和PDGF等因子,激活內(nèi)皮細胞的PI3K/Akt和Ras/MAPK信號通路,誘導(dǎo)血管內(nèi)皮細胞增殖、遷移和管腔形成。
- 此外,NSCs可通過釋放外泌體傳遞促血管生成miRNA(如miR-126),調(diào)控內(nèi)皮細胞的基因表達,進一步促進血管新生。
改善局部微循環(huán):臨床影像學研究(如功能性磁共振成像fMRI)表明,NSCs移植后,腦白質(zhì)損傷區(qū)的血流量顯著增加,局部血氧飽和度提高。這一改善與新生血管網(wǎng)絡(luò)的形成密切相關(guān),有助于恢復(fù)缺血區(qū)域的代謝支持,減少神經(jīng)元凋亡。
2.5 神經(jīng)可塑性與功能重組
移植的NSCs通過以下途徑增強神經(jīng)可塑性:
- 突觸重塑:旁分泌效應(yīng)促進突觸連接的重組,優(yōu)化神經(jīng)環(huán)路功能。
- 運動功能恢復(fù):2021年,海軍總醫(yī)院臨床研究表明,鞘內(nèi)或腦室內(nèi)移植NSCs后,患兒的粗大運動功能評分(GMFM)顯著提升,肌張力和步態(tài)明顯改善。
- 協(xié)同康復(fù)訓(xùn)練:NSCs修復(fù)的神經(jīng)網(wǎng)絡(luò)與康復(fù)訓(xùn)練形成正向反饋,加速運動及認知功能的恢復(fù)。
三、挑戰(zhàn)與未來方向
盡管機制明確,仍存在以下問題:
免疫排斥風險:異體NSCs可能引發(fā)宿主免疫反應(yīng),需通過HLA配型或免疫抑制劑降低風險。
細胞存活與功能維持:移植細胞的存活時長及基因表達穩(wěn)定性(如轉(zhuǎn)基因NSCs的療效衰減)需進一步優(yōu)化。
精準遞送技術(shù):經(jīng)鼻、鞘內(nèi)等非侵入性途徑可繞過血腦屏障,提高干細胞靶向遷移效率。
結(jié)語
神經(jīng)干細胞移植通過多機制協(xié)同作用,為腦癱治療提供了從結(jié)構(gòu)修復(fù)到功能恢復(fù)的綜合解決方案。隨著基因編輯技術(shù)和遞送方式的進步,未來有望實現(xiàn)更精準、持久的治療效果。
相關(guān)閱讀:神經(jīng)干細胞如何改寫腦癱治療?5大核心優(yōu)勢及臨床案例深度剖析
參考資料:
梁寶仁, 等.?“干細胞移植治療腦癱的研究進展.”?中國熱帶醫(yī)學?12.?08?(2012):?1020-1022+1032.
周菊花方素珍周細中綜述李,宏審校。 神經(jīng)干細胞移植治療重度腦癱的研究進展[J]. 臨床兒科雜志, 2014, 32(1): 85-87.
劉衛(wèi)鵬,屈素清,欒佐,等.人神經(jīng)前體細胞移植治療重度腦癱患兒療效觀察[J].中國當代兒科雜志,2012,14(10):759-762.
免責說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。




 掃碼添加官方微信
掃碼添加官方微信