2026年3月1日,《Diabetes & Metabolism》發表題為“干細胞治療糖尿病的主要臨床試驗概述”的研究綜述[1]。文章指出,基于干細胞的療法正引領糖尿病治療從癥狀控制邁向病因干預,其核心目標在于恢復胰島素分泌細胞的功能。干細胞療法重塑糖尿病治療格局已實現從供體胰島移植(如埃德蒙頓方案)向人多能干細胞來源的β細胞替代療法的關鍵跨越。

干細胞療法重塑糖尿病治療格局——主要臨床試驗概述與未來展望
一、全球健康挑戰與治療困境
糖尿病是21世紀最緊迫的全球性健康挑戰之一。患者規模持續攀升,預計到2025年將影響全球8.3億人,給各國醫療系統帶來沉重負擔。盡管藥物研發、胰島素輸注技術與血糖監測手段長足進步,但現有治療策略本質上仍屬姑息性,無法實現根治。
1型糖尿病患者需終身依賴外源性胰島素;2型糖尿病則面臨進行性β細胞功能障礙與胰島素抵抗的雙重困境。這些局限凸顯了開發再生療法的緊迫性——恢復內源性胰島素分泌,實現持久穩態的血糖控制,從根本上變革現有治療范式。

二、理論基礎與臨床前證據
在此背景下,基于人類多能干細胞(包括胚胎干細胞和誘導多能干細胞)及間充質干細胞的療法應運而生,成為最具前景的再生策略。這些干細胞具備分化為胰島素分泌細胞或調節免疫代謝通路的獨特能力,有望為糖尿病治療帶來范式轉變(圖1)。
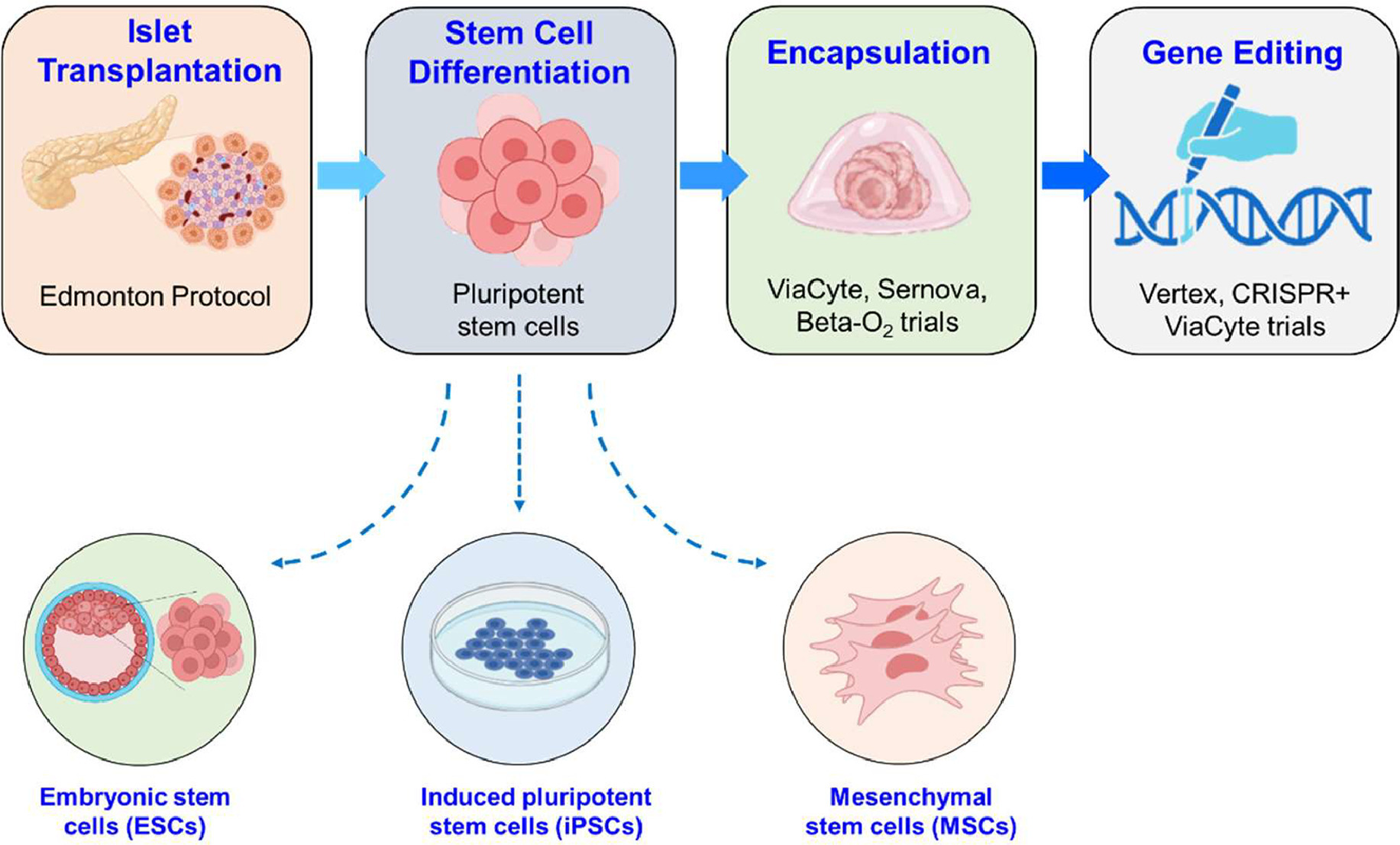
臨床前研究證實,通過定向分化技術可引導多能干細胞和胰腺祖細胞生成能響應葡萄糖刺激并分泌胰島素的β樣細胞。同時,間充質干細胞憑借其免疫調節與抗炎特性,展現出保護1型糖尿病患者殘余β細胞功能、改善2型糖尿病胰島素敏感性的潛力。
三、從實驗室到臨床:干細胞療法的里程碑式轉化
過去二十年間,這些臨床前研究的突破已成功轉化為日益增多的臨床試驗。具有里程碑意義的埃德蒙頓胰島移植方案驗證了β細胞替代療法的可行性,但其廣泛應用受限于供體短缺和免疫排斥(表1)。
| 干細胞 | 起源 | 分化潛能 | 優勢 | 局限性/挑戰 | 主要應用 | 參考 |
|---|---|---|---|---|---|---|
| 胰腺祖細胞 | 胰腺發育過程中的前腸內胚層 | 胰腺內分泌細胞(β、α、δ、PP)和外分泌細胞(腺泡、導管)。 | 與糖尿病治療直接相關的是產生胰島素的β細胞 | 難以分離和擴增;譜系限制了其更廣泛的應用。 | 糖尿病治療;胰腺再生;疾病建模 | [ 19 , 23 ] |
| 胚胎干細胞(ESCs) | 囊胚內細胞團(受精后4-5天) | 除胎盤外,可形成所有身體組織。 | 多能性的黃金標準;強大的分化能力 | 倫理考量;免疫排斥風險 | 發育生物學;再生醫學;細胞治療研究 | [ 19 , 33 ] |
| 誘導多能干細胞(iPSCs) | 重編程的成體體細胞(成纖維細胞;Oct4、Sox2、Klf4、c-Myc) | 可以分化成幾乎所有體細胞類型 | 避免了胚胎干細胞的倫理問題;針對特定患者;無限擴增 | 誘導效率低;存在遺傳不穩定和腫瘤發生的風險 | 疾病建模;藥物篩選;再生醫學 | [ 34 , 35 ] |
| 間充質干細胞(MSCs) | 成人組織(骨髓、脂肪組織、臍帶等) | 中胚層譜系:成骨細胞、軟骨細胞、脂肪細胞 | 易于分離;具有強大的免疫調節和抗炎特性;腫瘤風險低。 | 分化譜有限;供體間存在差異 | 骨科修復;心血管治療;免疫調節;組織工程 | [ [36] , [37] , [38] ] |
| 基因編輯細胞(低免疫原性PEC/β細胞) | 利用 hESCs/iPSCs 衍生的內分泌譜系進行基因工程改造(例如,通過 CRISPR 編輯 HLA) | β樣或胰腺內胚層經基因工程改造以逃避免疫反應 | 免疫原性降低;可采用同種異體“現成”策略 | 監管審查;免疫逃逸的持久性;脫靶風險 | 無需全身免疫抑制的同種異體β細胞替代療法 | [ [39] , [40] , [41] ] |
| 公司 | 成立年份/總部 | 領導項目 | 技術重點 | 臨床試驗狀態 | 要點 | 參考資料 |
|---|---|---|---|---|---|---|
ViaCyte | 1999年/美國圣地亞哥 | PEC-Encap(VC-01;NCT02265809) PEC-Direct(VC-02;NCT03163511) VCTX210A(PEC-QT;NCT05210530;采用 CRISPR 療法) | 胚胎干細胞衍生的胰腺祖細胞;封裝裝置;基因編輯的免疫逃逸細胞 | 1/2期臨床試驗已完成(PEC-Encap、PEC-Direct);PEC-QT處于早期臨床階段(2025年)。 | 2022年被Vertex以3.2億美元收購;干細胞衍生β細胞替代療法的先驅;封裝裝置面臨纖維化挑戰 | [ 42 , 43 ] |
Vertex制藥公司 | 1989年/美國波士頓 | VX-880(NCT04786262;Zimislecel) VX-264(TrialTroveID-492,327) | 誘導多能干細胞衍生的胰島素分泌細胞;門靜脈輸注;封裝裝置 | VX-264 處于早期臨床階段;VX-880 正在進行 1/2/3 期關鍵性試驗(2024-2025 年) | 首例患者于2021年實現胰島素非依賴性;VX-880有望在2026年提交監管審批。 | [ 44 , 45 ] |
Sernova公司 | 2008年/加拿大安大略省 | 細胞袋系統(Sernova 的細胞袋;NCT03513939) | 植入供體胰島或干細胞衍生β細胞的生物工程皮下囊袋 | Sernova公司用于治療性胰島移植的細胞袋的安全性和有效性的1/2期研究;中期數據顯示C肽生成和HbA1c<7.0%。 | 2025年更名為Sernova Biotherapeutics Inc.;已證實可促進血管生成并維持胰島細胞的長期存活;正在拓展平臺,開發干細胞衍生療法。 | [ 46 , 47 ] |
諾和諾德 | 1989年 / 丹麥巴格斯韋德 | 口服索馬魯肽治療 2 型糖尿病患者的心血管安全性研究 (NCT02692716); 新藥 NNC0363-1063 治療 1 型糖尿病患者的研究( NCT06685185 ) | 干細胞衍生的β細胞可用于治療1型糖尿病和2型糖尿病 | 已于2025年10月停止細胞療法研發工作。 | 已于2025年10月停止細胞療法研發工作。 | [ 48 , 49 ] |
在此基礎上,以ViaCyte、Vertex等為代表的眾多機構積極投身于干細胞衍生胰腺祖細胞、封裝裝置以及基因編輯免疫逃逸細胞系的臨床探索(表2)。2000年至2025年間,相關臨床試驗數量已超過150項,標志著該領域的研究熱情與快速發展,旨在克服傳統移植療法的瓶頸。
四、挑戰與未來方向
盡管進展令人鼓舞,干細胞療法邁向常規臨床仍面臨嚴峻挑戰:免疫排斥反應、移植細胞長期存活與功能維持、致瘤風險及大規模生產制造等均亟待攻克。封裝技術雖旨在保護移植物,但異物反應與血管化不足限制了其長期療效。科學家正積極探索基因編輯、生物工程等前沿手段,終極目標是在無需長期全身免疫抑制的條件下,實現患者的功能性治愈。
本文全面概述了2000年以來糖尿病干細胞療法的主要臨床試驗。通過綜合分析試驗設計、結果與局限性,旨在突出進展、剖析挑戰,并將當前研究置于再生醫學更廣闊的發展軌跡中,著重探討干細胞療法在未來數十年如何從實驗性前景走向常規臨床應用。
開發干細胞衍生糖尿病療法的關鍵要素
開發干細胞衍生糖尿病療法的關鍵要素,首先在于深刻理解其多靶點的治療機制,并以此為基礎設計臨床試驗。該療法并非僅通過單一途徑發揮作用,而是通過三種相互關聯的機制靶向糖尿病復雜的病理:直接分化為產生胰島素的β細胞以替代缺失的細胞、通過旁分泌信號促進內源性胰島再生,以及調節免疫系統以對抗自身免疫或炎癥損傷。
臨床前研究已在多種干細胞類型中證實了這些能力,但只有經過嚴格設計的臨床試驗,才能將這些實驗室發現轉化為確切的人體治療價值,驗證其在實際生理環境中的安全性和有效性(圖2)。
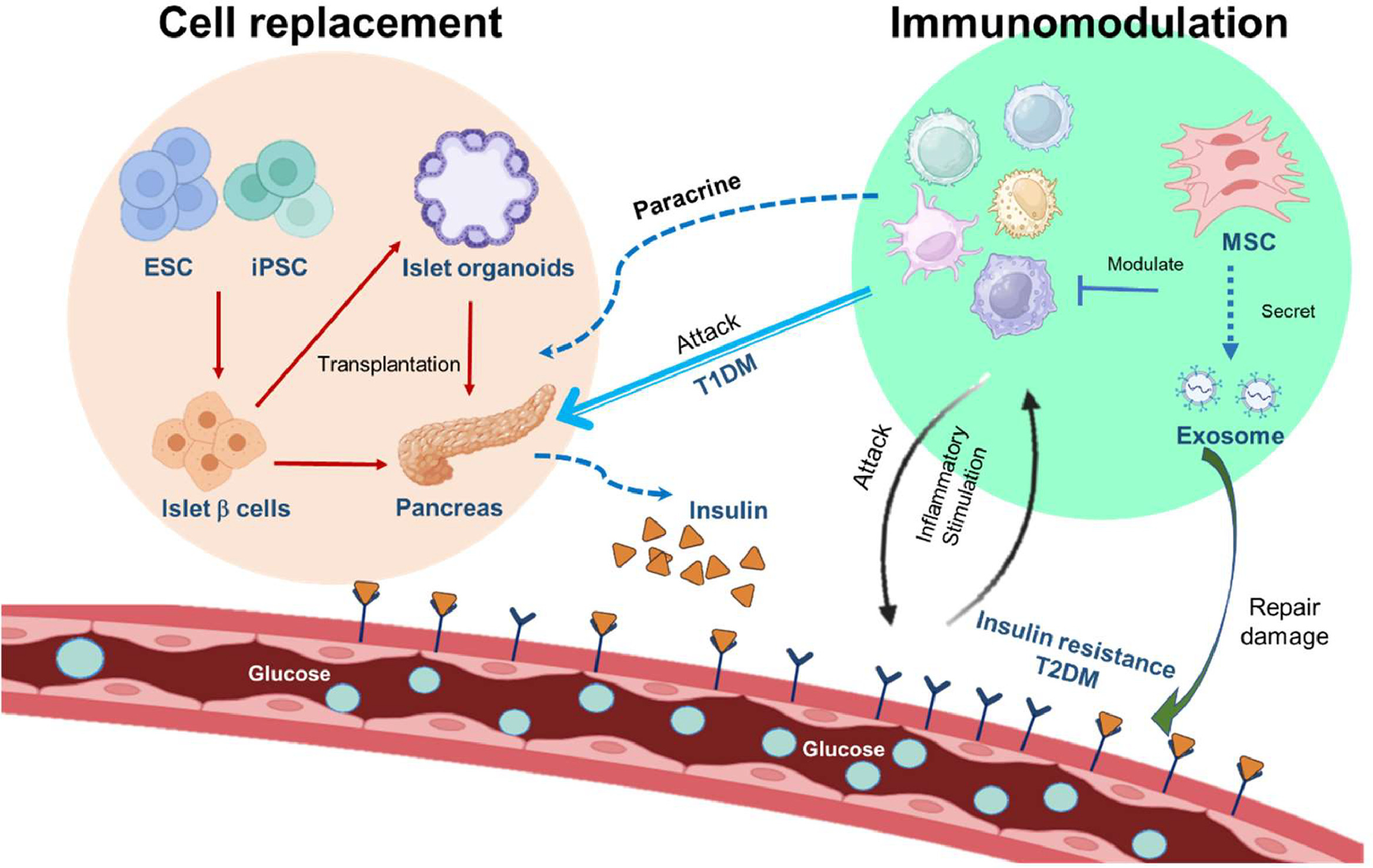
其次,借鑒并超越傳統的細胞替代療法經驗是推動發展的關鍵。供體胰島移植(如埃德蒙頓方案)的成功,證明了細胞療法可實現胰島素非依賴性并獲得監管批準,但其應用受限于供體短缺和免疫排斥。因此,基于干細胞的療法必須同時解決這兩個核心障礙。一方面,它旨在提供一種可再生的細胞來源,替代稀缺的供體胰島;另一方面,早期臨床試驗顯示干細胞可通過免疫調節發揮輔助治療作用,改善血糖控制,這提示了一種雙重策略:既通過分化細胞直接替代,又通過未分化細胞或其旁分泌作用調節病理環境,從而為1型或2型糖尿病提供更全面的治療路徑。
最后,臨床試驗的價值遠不止于驗證療效,更是推動療法從實驗室走向臨床成熟的迭代平臺。試驗不僅需建立標準化的療效終點(如糖化血紅蛋白降低、胰島素非依賴性),更要積累長期安全性數據、監測遠期風險。這些結果為監管路徑建立、生產標準統一及倫理框架協調提供關鍵信息。更重要的是,每一項臨床試驗均基于前人經驗教訓,不斷優化細胞制備工藝、移植方案及患者篩選標準。這種迭代進步是將干細胞療法塑造為安全、有效且可控的臨床手段,最終實現恢復葡萄糖穩態與修復胰腺功能根本目標的必由之路。
胚胎干細胞衍生療法治療糖尿病:從概念驗證到基因編輯
胚胎干細胞(ESCs)因其多能性與無限自我更新能力,長期被視為再生醫學的基石。在糖尿病領域,ESCs有望生成功能性胰島β細胞,恢復內源性胰島素分泌。21世紀初的開創性研究表明,ESCs可定向分化為胰腺譜系細胞,在體外產生表達胰島素的細胞,證實其可作為β細胞的可再生來源,有望克服尸源胰島移植的局限。
過去二十年,分化方案取得顯著進展。早期方法獲得的β樣細胞不成熟、葡萄糖反應性有限;逐步優化的分化方案模擬了胚胎胰腺發育過程,產生了功能性更強的細胞(表3)。2006年,D’Amour等人開發的五步方案將人ESCs轉化為功能性胰島素分泌細胞,這些細胞能產生多種胰腺激素,其來源的胰腺祖細胞在移植后表現出體內成熟能力,可在葡萄糖刺激下分泌胰島素并逆轉動物模型的高血糖。
美國ViaCyte公司引領了ESC衍生療法的臨床轉化,是首家將人ESC來源胰腺祖細胞(PP)推進臨床試驗的機構。其首款產品PEC-Encap(VC-01)將ESC來源胰腺祖細胞封裝于裝置內,旨在保護細胞免受免疫攻擊,同時允許營養物質交換。植入后,祖細胞能成熟為胰島素生成細胞。初步I/II期試驗證實了安全性與細胞存活率,但裝置周圍纖維化限制了長期療效。
為解決此問題,ViaCyte推出PEC-Direct(VC-02),直接植入祖細胞但需全身免疫抑制。早期試驗顯示,1型糖尿病患者體內可檢出C肽,證明細胞已分化為胰島素分泌細胞。最近,ViaCyte與CRISPR Therapeutics合作開發PEC-QT(VCTX210、VCTX211),利用基因編輯技術使ESC來源祖細胞逃避免疫排斥,旨在實現持久胰島素非依賴性且無需終身免疫抑制,標志著該領域的重大進展(表3)。
| 試驗名稱 | 開始年份 | 贊助 | 試驗目標 | 試驗/參與者編號 | 細胞類型 | 主要成果 | 影響 | 參考資料 |
|---|---|---|---|---|---|---|---|---|
| 胚胎干細胞衍生療法治療糖尿病 | ||||||||
| VC-01(PEC封裝) | 2014–2019 | ViaCyte | 包埋胰腺祖細胞的安全性和存活率 | 1型糖尿病(2)/約19 | ESCs衍生的胰腺內胚層細胞(PEC-01) | 證實細胞存活并部分成熟;檢測到C肽;纖維化限制了療效 | 封裝概念驗證;突出異物反應挑戰 | [ 24 , 57 ] |
| VC-02(PEC-Direct) | 2017–2022 | ViaCyte | 評估開放式裝置中的血管化和胰島素生成情況 | 1型糖尿病(1)/約15-20 | 胚胎干細胞衍生的胰腺祖細胞 | 血管生成改善;觀察到胰島素分泌;需要全身免疫抑制治療 | 已證實胰島素功能正常;但需權衡免疫抑制負擔。 | [ 58 , 59 ] |
| VCTX210A(免疫逃逸型PEC產品) | 2022–2024 | ViaCyte + CRISPR Therapeutics | 評估基因編輯的低免疫原性PEC細胞的安全性和移植效果 | T1DM(1)/ ~12 | ESCs衍生的胰腺內胚層細胞(PEC210A) | CRISPR基因編輯技術改造的免疫逃逸細胞首次人體試驗;安全性可接受;療效待定 | 基因編輯干細胞療法里程碑式試驗;有望消除免疫抑制 | [ 39 ] |
| VCTX211(下一代免疫逃逸型PEC) | 2023年至今 | ViaCyte + CRISPR Therapeutics | 工程化光電化學細胞的安全性、耐受性和有效性 | T1DM(1/2)/ ~30 | 胚胎干細胞來源的胰腺內胚層細胞 | 正在進行中;旨在提高耐久性和免疫逃避能力 | 有望建立可擴展的免疫保護干細胞療法 | [ 40 ] |
| iPSCs β樣療法治療糖尿病 | ||||||||
| VX-880(全身移植) | 2021年至今 | Vertex制藥公司 | 恢復內源性胰島素分泌;減少/停止胰島素注射 | 1 型糖尿病 ( 1 ) 伴低血糖感知障礙 / ~52 | iPSCs β樣細胞或胰腺祖細胞 | 早期患者C肽水平恢復正常,胰島素注射減少或停止;糖化血紅蛋白<7.0%;安全性良好 | 干細胞衍生胰島在人體中的概念驗證;顯示出療效,但需要終身免疫抑制 | [ 26 , 60 ] |
| VX-264(封裝式頂點療法) | 2013–2025 | Vertex制藥公司 | 采用封裝策略以避免全身免疫抑制 | 1型糖尿病(1/2)/ NA | iPSCs β樣細胞或胰腺祖細胞 | 早期試點工作已完成;目前正在進行以安全性和可行性為終點的試驗。 | 如果成功,可減輕免疫抑制負擔;解決封裝難題。 | [ 30 , 61 , 62 ] |
誘導多能干細胞療法治療糖尿病:從患者特異到通用型
誘導多能干細胞(iPSCs)的誕生為糖尿病細胞療法開辟了新路徑。通過導入特定轉錄因子將成體細胞重編程為多能狀態,既保留了與ESC相當的分化潛能,又規避了胚胎組織的倫理爭議。這一突破使構建患者特異性干細胞系成為可能,為自體移植減少免疫排斥奠定了基礎。研究者已成功將iPSCs定向誘導分化為胰腺譜系,獲得能響應葡萄糖刺激并分泌胰島素的成熟β樣細胞。
臨床轉化層面,Vertex Pharmaceuticals進展最具代表性。其核心產品VX-880通過門靜脈輸注移植iPSC衍生胰島素分泌細胞,2021年首例患者實現里程碑式的胰島素非依賴性。后續I/II期數據顯示,患者單次移植后恢復內源性胰島素分泌,C肽持續檢出,血糖控制顯著改善,外源性胰島素依賴大幅降低。但該方案仍需配合全身免疫抑制。為此Vertex推出VX-264,采用封裝裝置保護移植細胞,旨在消除終身免疫抑制的必要性,形成直接輸注與裝置封裝并行的雙重策略。
除國際領軍企業外,中國學術團隊亦取得突破。2024年,國內合作團隊發表首例化學誘導多能干細胞(CiPSCs)來源胰島移植臨床報告:將自體CiPSCs分化為胰島細胞,移植入1型糖尿病患者體內,成功實現功能性胰島素非依賴。這一成果驗證了化學重編程路線的可行性,為減少供體依賴、降低免疫抑制需求提供了新的臨床證據。
盡管iPSCs衍生療法前景廣闊,仍面臨多重挑戰:大規模生產符合GMP標準的iPSC衍生β細胞需嚴格質控體系以消除致瘤風險;移植細胞長期存活與功能維持有賴于生物材料、血管化策略及免疫調節技術的持續優化。盡管如此,iPSCs技術因其個性化、符合倫理及潛在規模化應用前景,仍被視為實現全球可推廣糖尿病治療的重要路徑。
間充質干細胞療法:從細胞治療到無細胞制劑
間充質干細胞(MSCs)是糖尿病領域研究最為廣泛的干細胞類型之一。其優勢在于易于獲取、免疫原性低及強大的免疫調節與旁分泌作用。與ESC或iPSC不同,MSCs是來源于骨髓、脂肪、臍帶或牙髓的成體祖細胞,其治療應用并非主要基于直接分化為胰島素分泌細胞,而是通過調節免疫微環境、改善代謝發揮效用。
臨床試驗已證實MSCs可改善1型及2型糖尿病患者的代謝指標。Hu等報道,1型糖尿病患者靜脈輸注異體MSCs可提高C肽水平、降低胰島素需求。Xu等通過薈萃分析證實,MSCs療法安全有效,可適度改善血糖控制。Zang等報道,MSCs治療顯著改善1型糖尿病患者C肽水平并降低胰島素需求。進一步研究表明,臍帶來源MSCs可增強2型糖尿病患者血糖控制、降低HbA1c。
近年來,該領域正經歷從“細胞治療”向“無細胞治療”的范式演進。MSC來源外泌體作為新型治療劑,能遞送調節免疫與代謝通路的生物活性分子,規避全細胞療法的致瘤風險,提高產品可重復性與規模化生產潛力。早期臨床探索如Exo-HWS試驗正驗證這一方向可行性。然而,MSCs療法仍面臨諸多挑戰:直接替代β細胞能力有限、產品異質性大、治療效果可能短暫需重復給藥、臨床應用標準化面臨監管障礙。
展望未來,MSCs療法的價值將更多體現在聯合治療策略中。其免疫調節與代謝支持功能有望與ESC/iPSC來源β細胞替代療法形成協同,在實現胰島素分泌重建的同時,為移植細胞提供免疫保護微環境。推動MSC來源外泌體等無細胞制劑的標準化與規模化生產,開展大規模隨機對照試驗驗證其長期療效與安全性,將是該領域走向臨床成熟的關鍵路徑。MSCs雖難以獨立實現治愈,但注定將成為糖尿病綜合干細胞治療策略中不可或缺的組成部分。
用于干細胞治療糖尿病的封裝技術
封裝技術:從物理屏障到免疫逃逸
封裝技術在干細胞衍生糖尿病療法中扮演著免疫保護的核心角色。它通過生物材料構建物理屏障,將移植細胞與宿主免疫系統隔離,從而避免或減少對全身免疫抑制的依賴。這種屏障在保護細胞的同時,允許氧氣、營養物質、葡萄糖及胰島素等小分子自由雙向擴散,確保細胞能感知血糖變化并響應性分泌胰島素。該技術旨在破解供體稀缺與終身免疫抑制兩大瓶頸,目前主要形成宏觀封裝(可回收裝置)與微觀封裝(水凝膠包裹)兩大策略。
臨床應用中,封裝技術經歷了顯著迭代(圖3)。最具代表性的ViaCyte公司PEC-Encap(VC-01)率先將ESC來源胰腺祖細胞封裝植入人體,早期試驗證實安全性,但裝置誘發的異物反應導致纖維化與血管化不足,限制了細胞存活。為規避此問題,ViaCyte一方面推出需配合免疫抑制的PEC-Direct(VC-02),另一方面與CRISPR Therapeutics合作開發PEC-QT,通過基因編輯賦予細胞免疫逃逸能力。其他創新平臺如Sernova的Cell Pouch System側重于在植入前構建血管化組織微環境;Beta-O2 Technologies的βAir裝置則通過集成氧氣室維持細胞活力。

從技術演進看,封裝技術正從單純的物理屏障向生物工程與基因編輯相融合的復合型平臺發展。早期技術聚焦于用半透膜保護供體胰島;隨后研究重點轉向開發生物相容性更好、能有效減少纖維化并促進血管化的新材料;最新突破方向是將基因編輯技術引入,構建具有免疫逃逸能力的干細胞衍生β細胞,實現再生醫學與生物工程的深度融合。這一演進路徑的終極目標,是在無需全身免疫抑制條件下,利用可再生干細胞來源實現規模化、持久且安全的胰島素非依賴性治療。
未來干細胞治療糖尿病的挑戰都有哪些?
首先,在科學與技術層面,免疫排斥和安全性是根本性障礙。即使使用自體誘導多能干細胞(iPSC)衍生的β細胞,在1型糖尿病自身免疫背景下,移植細胞仍可能被機體原有的免疫記憶攻擊。致瘤性風險同樣嚴峻,若多能干細胞分化不完全,殘留的未分化細胞可能導致畸胎瘤形成,因此需要開發極致的純化和安全檢測技術。此外,如何確保大規模生產的每一批次β細胞都具有成熟的功能性和葡萄糖反應性,以及如何解決移植后細胞因纖維化包裹、氧合不足和血管化不良而導致的長期存活率低下,都是亟待突破的技術瓶頸。
| 挑戰 | 影響 | 潛在解決方案 | 參考 |
|---|---|---|---|
| 免疫排斥 | 移植細胞丟失;需要免疫抑制治療 | 基因編輯(CRISPR/Cas9);封裝裝置;免疫療法;通用供體細胞系 | [ 22 , 24 ] |
| 致瘤性 | 安全風險(畸胎瘤形成、遺傳不穩定性) | 純化;嚴格的質量控制;自殺基因(誘導型caspase-9);基因組穩定性檢測 | [ 98 , 99 ] |
| 分化變異性 | 胰島素分泌不穩定;細胞群體異質性 | 標準化方案;生物反應器優化;類器官系統;階段特異性生長因子 | [ 35 , 100 ] |
| 長期生存 | 由于缺氧、纖維化和炎癥導致移植腎功能下降 | 先進生物材料;血管化策略;與間充質干細胞共移植;抗纖維化支架 | [ 24 , 99 ] |
| 生產規模 | 全球準入受限且成本高昂 | 可擴展的生物工藝;自動化;封閉式GMP生產;國際細胞庫 | [ 98 ] |
| 監管和倫理問題 | 臨床應用緩慢、全球標準分散、公眾接受度低以及道德爭議 | 優先選擇誘導多能干細胞來源;替代捐贈者來源;統一的國際準則;透明的治理框架; | [ 3 , 52 , 98 , 99 ] |
其次,在生產、臨床轉化與監管層面,標準化和可及性面臨巨大挑戰。全球范圍內對數以十億計功能性β細胞的需求,要求建立符合良好生產規范的超大規模擴增體系。目前尚缺乏國際公認的效力、純度和安全性評估檢測方法,導致不同臨床試驗間的終點指標(如糖化血紅蛋白降低與胰島素完全依賴)難以橫向比較。各地區碎片化的監管審批框架和漫長的審查流程,進一步延緩了療法的轉化應用。封裝裝置雖有望解決免疫排斥,但其自身也面臨著纖維化過度、氧合不足以及長期生物相容性和耐久性等工程設計難題。
最后,在疾病特異性和倫理層面,治療策略需要精準匹配病理機制。1型糖尿病必須解決自身免疫復發問題,這意味著單純的細胞替代可能需要聯合免疫調節策略;而2型糖尿病則需要應對全身性胰島素抵抗,否則移植的β細胞可能因代謝負荷過重而失效。此外,圍繞胚胎干細胞使用的倫理爭議,包括供體組織來源、患者知情同意和公平獲取醫療資源等問題,依然是必須審慎應對的社會議題。克服這些挑戰,需要細胞工程、生物材料、規模化生產和個性化醫療策略的協同進步。
未來干細胞治療糖尿病的方向
基于干細胞的糖尿病治療未來將深度融合基因編輯、生物材料與組織工程,致力于開發能夠逃避免疫攻擊的“通用型”細胞產品。以CRISPR/Cas9技術為核心的免疫逃逸干細胞是當前最活躍的研究方向,通過敲除移植細胞的免疫識別位點,使其在不需或僅需極少免疫抑制的情況下長期存活(圖4)。

ViaCyte與CRISPR Therapeutics合作的PEC-QT項目以及CTX211等產品已進入早期臨床試驗,旨在驗證這一策略的可行性。與此同時,封裝技術正從單純的物理屏障向智能化、功能化平臺演進,新一代裝置將整合免疫調節涂層、促血管化設計和實時生物傳感功能,以解決纖維化包裹和氧合不足等關鍵難題,最終實現無需免疫抑制的胰島素非依賴性。
| 未來方向 | 關鍵創新 | 預期影響 | 示例 | 參考資料 |
|---|---|---|---|---|
| 免疫逃逸干細胞 | 經 CRISPR 編輯的具有多基因免疫隱蔽功能的 β 細胞(例如,B2M/CIITA 敲除;HLA-E/HLA-G/PD-L1 過表達);NK/T 細胞活化降低的“隱形”胰島 | 無需維持免疫抑制即可擺脫胰島素依賴;排斥反應發生率更低;適用范圍更廣,包括兒童1型糖尿病患者。 | ViaCyte-CRISPR PEC-QT (VCTX210);通用低免疫原性iPSCs細胞系;HLA工程學術聯盟 | [ 111 , 112 ] |
| 封裝 | 抗纖維化、兩性離子和聚乙二醇化生物材料;巨噬細胞重編程涂層;氧合/血管生成裝置設計;具有優化傳質的微/宏囊化 | 長期移植存活率高,異物反應降低;血糖控制穩定;可回收性好且安全 | ViaCyte PEC-Encap;Sernova細胞囊;藻酸鹽變體(三唑/氟化藻酸鹽);產氧支架 | [ 113 , 114 ] |
| 制造業 | 符合GMP標準的封閉式工作流程;具備在線監測功能的自動化區分;可擴展的攪拌罐/灌注式生物反應器;穩健的釋放和效力檢測 | 可擴展的全球療法,批次可重復;更低的藥品成本;更快的批次放行速度和供應可靠性 | 立式輪式攪拌罐生物反應器;標準化的β細胞分化標準操作規程;質量控制指標(C肽分泌、葡萄糖反應性、無菌性、核型) | [ [115] , [116] , [117] ] |
| 聯合療法 | 間充質干細胞共移植用于免疫調節;Treg細胞誘導;抗原特異性耐受(例如,耐受性樹突狀細胞);β細胞替代加免疫重置(例如,低劑量生物制劑) | 療效增強,自身免疫反應和移植失敗率降低;移植成功率和血管化改善;低血糖事件減少 | 間充質干細胞+胰島替代療法試點研究;基于調節性T細胞的耐受性試驗;輔助低劑量抗CD3/IL-2療法 | [ 29 , 38 , 118 ] |
| 生物工程 | 血管化胰島構建體的3D生物打印;芯片類器官微流控技術;用于快速灌注的內皮細胞和周細胞共培養;智能生物傳感器集成 | 構建具有生理胰島素動力學、更佳耐久性和實時監測功能的生物工程胰腺 | 生物打印胰島支架;芯片胰島平臺;具有內皮網絡的血管化類器官 | [ 119 , 120 ] |
| 臨床擴展 | 采用標準化終點指標(C肽曲線下面積、血糖達標時間、嚴重低血糖發生率、外源性胰島素減少量)的II/III期多中心試驗;長期安全性注冊研究 | 監管部門批準和全球推廣;支付方覆蓋范圍;來自不同人群的證據 | Vertex VX-880/VX-264 試驗;ViaCyte 項目;持久療效的協調注冊研究 | [ 61 ] |
| 政策框架 | 細胞療法的國際統一監管;加速審批途徑(RMAT、PRIME、Sakigake);上市后承諾;符合倫理的采購和公平獲取模式 | 更快、更安全的翻譯;全球標準化;公平分配和價格合理 | FDA RMAT、EMA PRIME、PMDA Sakigake;WHO/ISCT 指南;基于價值的報銷試點項目 | [ 121 ] |
在生產與制造層面,實現大規模、可重復且標準化的細胞生產是未來十年臨床轉化的核心任務。隨著誘導多能干細胞(iPSC)技術的成熟,治療模式將呈現患者特異性與通用型供體細胞并存的格局。生物反應器系統的開發旨在穩定生成數十億級的功能性胰島β細胞,以滿足全球日益增長的患者需求。同時,國際社會亟需統一分化方案、效力檢測與安全性評估標準,確保不同地區、不同中心生產的細胞產品具有一致的質量和療效。3D生物打印與胰腺類器官技術的進步,將進一步推動構建具有復雜血管結構和微環境的可移植組織,為實現完全生物工程化胰腺替代奠定基礎。
面對糖尿病復雜的病理機制,聯合治療策略將成為提升療效的關鍵方向。將間充質干細胞(MSC)與ESC/iPSC衍生的β細胞聯合應用,可同時發揮免疫調節、旁分泌支持與胰島素分泌的協同作用。此外,干細胞移植與免疫療法(如檢查點抑制劑、耐受性疫苗)的組合,有望預防1型糖尿病患者自身免疫病的復發。針對2型糖尿病,干細胞治療則需與生活方式干預或代謝藥物相結合,以克服胰島素抵抗對移植細胞功能的影響。這些多維度的聯合策略體現了從單純細胞替代向系統功能重建的理念轉變。
最終,干細胞治療糖尿病的未來發展高度依賴于政策創新、倫理框架完善與全球化協作。開展大規模多中心3期臨床試驗,驗證療法的長期安全性、有效性及持久性,并建立包括胰島素非依賴性、糖化血紅蛋白降低和低血糖預防在內的標準化終點指標,是獲得監管批準的必要條件。同時,政策制定者需推動監管框架的國際協調,解決胚胎干細胞使用、供者知情同意、治療公平可及等倫理議題。
展望未來,根據文本提供的路線圖,該領域正沿著“2025年免疫保護創新→2030年可擴展生產→2035年監管優化→2040年治愈性療法”的軌跡演進,最終通過再生醫學、生物工程與政策創新的融合,實現持久胰島素非依賴性和全球可及的變革性目標。
結論
臨床證據已明確證實干細胞療法的潛力與局限。一方面,胰島移植的成功(如埃德蒙頓方案)及Vertex公司VX-880項目實現胰島素非依賴的案例,確證了通過細胞替代恢復胰島素分泌功能的可行性。另一方面,供體極度短缺、需終身使用免疫抑制劑、移植細胞長期存活率低以及1型糖尿病中自身免疫可能復發等問題,構成了臨床轉化的核心障礙。間充質干細胞的臨床研究雖展示了其免疫調節與代謝支持的輔助價值,但其本身無法替代胰島素生成,凸顯了單純依靠MSCs的局限性。
要實現常規臨床應用,必須克服技術、生產和監管的系統性挑戰。未來的關鍵在于將基因編輯(如CRISPR技術構建免疫逃逸細胞)、先進封裝技術(解決免疫排斥與細胞存活)和規模化生物反應器生產進行深度融合。產業界正積極投入這些方向——市場預測顯示,該領域將從2024年的約52億美元增長至2033年的128億美元。然而,最終成功還取決于開展設計嚴謹的III期臨床試驗以驗證長期療效與安全性,并建立全球統一的監管標準和倫理框架,確保治療的可及性與公平性。
參考資料:[1]:https://www.sciencedirect.com/science/article/abs/pii/S1262363626000170
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加官方微信
掃碼添加官方微信