隨著21世紀(jì)細(xì)胞療法的迅速發(fā)展,間充質(zhì)干細(xì)胞(Mesenchymal Stem Cells, MSCs)因其獨(dú)特的多向分化潛能和免疫調(diào)節(jié)特性,在治療多種難治性疾病方面展現(xiàn)了巨大的潛力。
2025年1月2日,中國(guó)國(guó)家藥監(jiān)局(NMPA)批準(zhǔn)鉑生卓越生物科技(北京)有限公司的艾米邁托賽注射液(商品名:睿鉑生)上市,中國(guó)迎來(lái)了第一款正式獲批的干細(xì)胞治療藥物。也標(biāo)志著全球已有16款間充質(zhì)干細(xì)胞藥物獲得批準(zhǔn)上市。
這些藥物不僅為某些傳統(tǒng)治療方法難以奏效的病癥帶來(lái)了新的希望,同時(shí)也引發(fā)了公眾對(duì)其成本效益和社會(huì)可及性的廣泛關(guān)注。本文將深入解析這些已上市間充質(zhì)干細(xì)胞藥物的價(jià)格及其所能治療的具體疾病。

全球已獲批上市的16款間充質(zhì)干細(xì)胞藥品價(jià)格與治療疾病全揭秘!
接下來(lái),我們來(lái)盤(pán)點(diǎn)全球已知上市的16款間充質(zhì)干細(xì)胞藥物。
其中,10款來(lái)源于骨髓,3款來(lái)源于臍帶,2款來(lái)源于脂肪,1款來(lái)源于臍帶血。
Mesoblast公司產(chǎn)品
1.Prochymal
從Prochymal到Ryoncil的研發(fā)歷程,歷經(jīng)美國(guó)、加拿大、澳大利亞和日本,間隔12年,最終成為FDA批準(zhǔn)的首款間充質(zhì)干細(xì)胞藥物。
- 批準(zhǔn)國(guó)家:加拿大
- 批準(zhǔn)日期:2012年5月17日
- 細(xì)胞類型:骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:兒童急性移植物抗宿主病(GvHD)
- 價(jià)格:20萬(wàn)美元/療程(通常4劑)
- 銷量:不詳
- 概況:Prochymal是一種即用型干細(xì)胞產(chǎn)品,可以通過(guò)簡(jiǎn)單的靜脈注射進(jìn)行輸注,無(wú)需進(jìn)行配型或免疫抑制。在美國(guó)通過(guò)擴(kuò)展訪問(wèn)程序可用,此外還在新西蘭、瑞士等國(guó)獲得批準(zhǔn)。
Prochymal于2009年首次在美國(guó)獲得批準(zhǔn),隨后被Osiris公司出售給澳大利亞的Mesoblast公司,并更名為Ryoncil。
2.Temcell
- 批準(zhǔn)國(guó)家:日本
- 批準(zhǔn)日期:2015年9月
- 細(xì)胞類型:骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:急性移植物抗宿主病(GvHD)
- 價(jià)格:868,680日元(約合7,700美元)/袋,一個(gè)標(biāo)準(zhǔn)療程通常需要8袋,因此總費(fèi)用約合12.3萬(wàn)美元)到18.5萬(wàn)美元。
- 銷量:2024年10月30日財(cái)報(bào)顯示,當(dāng)季銷售15億日元(約950萬(wàn)美元)
- 概況:Temcell是由Mesoblast公司開(kāi)發(fā),日本JCR制藥公司銷售。Temcell在臨床試驗(yàn)中顯示出良好的療效,特別是在治療類固醇難治性急性移植物抗宿主病方面。根據(jù)臨床數(shù)據(jù),接受Temcell治療的患者在28天后的總體反應(yīng)率達(dá)到56%。
其前身是Prochymal,由Mesoblast公司推動(dòng)上市。此外,Temcell還被納入日本國(guó)民健康保險(xiǎn)體系,這使得患者在治療時(shí)可以享受部分費(fèi)用報(bào)銷,從而降低了實(shí)際支付負(fù)擔(dān)。

3.Ryoncil
- 批準(zhǔn)國(guó)家:美國(guó)
- 批準(zhǔn)日期:2024年12月18日
- 細(xì)胞類型:骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:用于治療2個(gè)月及以上兒童的類固醇難治性急性移植物抗宿主病(SR-aGVHD)。
- 價(jià)格:尚未公開(kāi)
- 概況:這是FDA批準(zhǔn)的首個(gè)間充質(zhì)干細(xì)胞(MSC)療法。在一項(xiàng)多中心、單臂的III期臨床試驗(yàn)中,70%的患者在接受Ryoncil治療28天后顯示出總體反應(yīng),這一指標(biāo)與生存率相關(guān)。
由Mesoblast公司研發(fā)。Ryoncil作為一種創(chuàng)新的間充質(zhì)干細(xì)胞治療產(chǎn)品,為類固醇難治性急性移植物抗宿主病患者提供了新的治療選擇,并在未來(lái)有望擴(kuò)展到其他適應(yīng)癥。

韓國(guó)產(chǎn)品
作為擁有最多間充質(zhì)干細(xì)胞藥物的國(guó)家之一,韓國(guó)在過(guò)去10年內(nèi)未有新產(chǎn)品獲批,而現(xiàn)有產(chǎn)品的市場(chǎng)表現(xiàn)也大相徑庭。
4.CellGram
- 批準(zhǔn)國(guó)家:韓國(guó)
- 批準(zhǔn)日期:2011年7月1日
- 細(xì)胞類型:自體骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:急性心肌梗死(AMI)
- 價(jià)格:1800萬(wàn)韓元(約合15,000美元),且不在醫(yī)保報(bào)銷范圍內(nèi)。
- 銷量:2018年,達(dá)到25億韓元的峰值,隨后開(kāi)始下降,2023年為8億韓元。
- 概況:CellGram被認(rèn)為是全球首個(gè)獲得批準(zhǔn)的干細(xì)胞藥物,標(biāo)志著干細(xì)胞治療領(lǐng)域的重要里程碑。在臨床試驗(yàn)中,接受CellGram治療的患者在6個(gè)月后顯示左心室射血分?jǐn)?shù)提高了約6%。
CellGram上市時(shí)需在6年內(nèi)提供600名患者的臨床數(shù)據(jù)。Pharmicell后來(lái)申請(qǐng)將數(shù)量減至60人但被拒絕。這一情況引發(fā)了行業(yè)對(duì)其未來(lái)批準(zhǔn)狀態(tài)的關(guān)注。2022年,CellGram被重新評(píng)估為先進(jìn)生物制藥產(chǎn)品,表明其在監(jiān)管政策下仍具備一定的發(fā)展?jié)摿Α?/p>

5.Cartistem
- 批準(zhǔn)國(guó)家:韓國(guó)
- 批準(zhǔn)日期:2012年1月
- 細(xì)胞類型:臍帶血間充質(zhì)干細(xì)胞
- 適應(yīng)癥:退行性關(guān)節(jié)炎和膝關(guān)節(jié)軟骨損傷
- 價(jià)格:1.9-2.1萬(wàn)美元
- 銷量:累計(jì)給藥患者人數(shù)突破3.1萬(wàn),累計(jì)銷售額達(dá)到1080億韓元,2023年超過(guò)200億韓元(約1440萬(wàn)美元)。
- 概況:Cartistem 是世界上第一個(gè)同種異體臍帶血干細(xì)胞療法,已證明其在抑制炎癥和再生受損軟骨組織方面的有效性。
Medipost正在準(zhǔn)備Cartistem在日本和美國(guó)的3期臨床試驗(yàn),還計(jì)劃進(jìn)入馬來(lái)西亞等東盟國(guó)家。在日本,滿足條件可以跳過(guò)1、2期臨床試驗(yàn),直接進(jìn)入3期。

6.Cupistem
- 批準(zhǔn)國(guó)家:韓國(guó)
- 批準(zhǔn)日期:2012年1月
- 細(xì)胞類型:自體脂肪間充質(zhì)干細(xì)胞
- 適應(yīng)癥:克羅恩病的復(fù)雜性肛瘺
- 價(jià)格:約600萬(wàn)韓元(約5000美元/次)
- 銷量:未公開(kāi)
- 概況:Cupistem的一個(gè)顯著特點(diǎn)是其療效的持續(xù)性。在接受治療的患者中,81%在96周后仍保持愈合狀態(tài)。Cupistem于2014年獲得了韓國(guó)健康保險(xiǎn)審查與評(píng)估服務(wù)(HIRA)的醫(yī)療保險(xiǎn)價(jià)格批準(zhǔn),使得患者在經(jīng)濟(jì)上能夠更容易接受該治療。
7.NeuroNATA-R
- 批準(zhǔn)國(guó)家:韓國(guó)
- 批準(zhǔn)日期:2014年7月30日
- 細(xì)胞類型:自體骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:肌萎縮側(cè)索硬化癥(ALS)和其他運(yùn)動(dòng)神經(jīng)元病
- 價(jià)格:1.8萬(wàn)至7.2萬(wàn)美元
- 銷量:未公開(kāi)
- 概況:NeuroNATA-R通過(guò)注射自體骨髓間充質(zhì)干細(xì)胞,具有神經(jīng)保護(hù)作用,可以延緩運(yùn)動(dòng)神經(jīng)元的死亡,從而減緩ALS的進(jìn)展。在評(píng)估安全性的I期臨床試驗(yàn)中,共有7位患者接受了鞘內(nèi)注射,隨訪12個(gè)月,結(jié)果顯示該治療方案具有良好的安全性。
印度產(chǎn)品
8.Stempeucel
- 批準(zhǔn)國(guó)家:印度、歐盟
- 批準(zhǔn)日期:2015年6月(在歐盟獲得孤兒藥地位)
- 細(xì)胞類型:骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:嚴(yán)重肢體缺血價(jià)格:2200美元(2017年)
- 銷量:未公開(kāi)
- 概況:Stempeucel的研發(fā)歷時(shí)12年,采用獨(dú)特的池化技術(shù)(pooling technology),使得生產(chǎn)過(guò)程更高效,能夠?yàn)榇罅炕颊咛峁┲委煛ER床試驗(yàn)表明,Stempeucel在改善嚴(yán)重肢體缺血患者的血流和功能方面具有顯著效果。
日本產(chǎn)品
9.Alofisel
- 批準(zhǔn)國(guó)家:歐盟、日本
- 批準(zhǔn)日期:2018年3月23日(在歐盟獲得批準(zhǔn)),隨后在日本也獲得了批準(zhǔn)。
- 細(xì)胞類型:脂肪間充質(zhì)干細(xì)胞
- 適應(yīng)癥:復(fù)雜性肛瘺
- 價(jià)格:562萬(wàn)日元/劑(約3.6萬(wàn)美元)
- 銷量:2020財(cái)政年度,Takeda從Alofisel獲得的收入約35萬(wàn)美元。
- 概況:Alofisel在臨床試驗(yàn)中顯示出良好的安全性,但最近的一項(xiàng)研究表明其效果與安慰劑相當(dāng),因此其臨床效益受到質(zhì)疑。2024年12月,歐盟決定撤回Alofisel的市場(chǎng)授權(quán),原因是未能提供足夠的數(shù)據(jù)以確認(rèn)其療效。
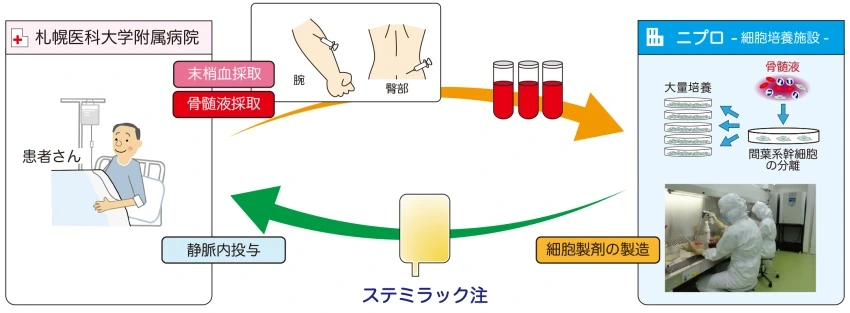
10.Stemirac
- 批準(zhǔn)國(guó)家:日本
- 批準(zhǔn)日期:2018年11月21日(獲得條件性和時(shí)間限制的批準(zhǔn))
- 細(xì)胞類型:骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:脊髓損傷相關(guān)的神經(jīng)功能障礙
- 價(jià)格:約1500萬(wàn)日元/劑(9.5萬(wàn)美元)
- 銷量:據(jù)2019年的一篇文章預(yù)測(cè),Stemirac將在未來(lái)9年中,每年給Nipro公司帶來(lái)約340萬(wàn)美元的收入。
- 概況:Stemirac在日本獲得了條件性和時(shí)間限制的批準(zhǔn),允許其在市場(chǎng)上銷售,同時(shí)要求Nipro公司在七年內(nèi)提供進(jìn)一步的臨床數(shù)據(jù)以證明其有效性。Stemirac在臨床試驗(yàn)中顯示出良好的安全性,被日本政府認(rèn)定為突破性產(chǎn)品,旨在加速其上市過(guò)程,以便為急需治療的患者提供新的選擇。
11.AKUUGO
- 批準(zhǔn)國(guó)家:日本
- 批準(zhǔn)日期:2024年7月31日(獲得條件性和時(shí)間限制的批準(zhǔn))
- 細(xì)胞類型:骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:改善創(chuàng)傷性腦損傷(TBI)引起的慢性運(yùn)動(dòng)癱瘓
- 價(jià)格:尚未公開(kāi)
- 銷量:尚未公開(kāi)
- 概況:AKUUGO是一種同種異體間充質(zhì)干細(xì)胞產(chǎn)品。它通過(guò)將人Notch-1胞內(nèi)結(jié)構(gòu)域基因暫時(shí)轉(zhuǎn)染到培養(yǎng)細(xì)胞中,增強(qiáng)了再生神經(jīng)細(xì)胞的能力。研究結(jié)果表明,AKUUGO不僅具有神經(jīng)保護(hù)作用,還能促進(jìn)血管生成并發(fā)揮免疫調(diào)節(jié)功能。

伊朗產(chǎn)品
12.Mesestrocell
- 批準(zhǔn)國(guó)家:伊朗
- 批準(zhǔn)日期:2018年
- 細(xì)胞類型:骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:骨關(guān)節(jié)炎
- 價(jià)格:2億伊朗里亞爾(約4600美元)
13.StemSin
- 批準(zhǔn)國(guó)家:伊朗
- 批準(zhǔn)日期:2018年
- 細(xì)胞類型:骨髓間充質(zhì)干細(xì)胞
- 適應(yīng)癥:多發(fā)性硬化癥
- 價(jià)格:未公開(kāi)
14.AlloStemSin
- 批準(zhǔn)國(guó)家:伊朗
- 批準(zhǔn)日期:2018年
- 細(xì)胞類型:臍帶間充質(zhì)干細(xì)胞
- 適應(yīng)癥:肌萎縮側(cè)索硬化癥
- 價(jià)格:未公開(kāi)
15.Vartocell
- 批準(zhǔn)國(guó)家:伊朗
- 批準(zhǔn)日期:2020年
- 細(xì)胞類型:臍帶間充質(zhì)干細(xì)胞
- 適應(yīng)癥:腦癱
- 價(jià)格:1億伊朗里亞爾(每瓶含2000萬(wàn)個(gè)細(xì)胞)約2300美元
中國(guó)產(chǎn)品
16.艾米邁托賽注射液
- 批準(zhǔn)國(guó)家:中國(guó)
- 批準(zhǔn)日期:2025年1月2日
- 細(xì)胞類型:臍帶間充質(zhì)干細(xì)胞
- 適應(yīng)癥:用于14歲以上患者的激素治療失敗的急性移植物抗宿主病(aGVHD),尤其是消化道受累為主的病例。
- 價(jià)格:尚未公開(kāi)
- 概況:這是中國(guó)首款獲得批準(zhǔn)的干細(xì)胞治療藥物,標(biāo)志著國(guó)內(nèi)干細(xì)胞藥物研發(fā)的重要里程碑。艾米邁托賽注射液通過(guò)利用人臍帶間充質(zhì)干細(xì)胞修復(fù)受損組織和調(diào)節(jié)免疫功能,在臨床試驗(yàn)中顯示出顯著的療效和安全性。
該藥物是通過(guò)中國(guó)國(guó)家藥監(jiān)局的優(yōu)先審評(píng)審批程序獲得上市的,意味著其在臨床上具有明顯的需求和潛在優(yōu)勢(shì)。它將作為處方藥在醫(yī)院使用,為患者提供新的治療選擇。
展望未來(lái)
盡管目前間充質(zhì)干細(xì)胞藥物的數(shù)量有限,但隨著科學(xué)研究的深入和技術(shù)的進(jìn)步,預(yù)計(jì)未來(lái)將有更多基于MSC的產(chǎn)品進(jìn)入市場(chǎng),進(jìn)一步擴(kuò)大其臨床應(yīng)用范圍。
同時(shí),如何平衡藥物創(chuàng)新與患者負(fù)擔(dān)之間的關(guān)系,確保安全有效的細(xì)胞治療能夠惠及更廣泛的人群,將是行業(yè)內(nèi)外共同面臨的挑戰(zhàn)。為了促進(jìn)這一領(lǐng)域的健康發(fā)展,各國(guó)政府和監(jiān)管機(jī)構(gòu)也在不斷優(yōu)化審批流程和支持政策,以加快優(yōu)質(zhì)產(chǎn)品的上市速度并降低患者的經(jīng)濟(jì)門(mén)檻。
結(jié)論
綜上所述,全球已上市的16款間充質(zhì)干細(xì)胞藥物不僅展示了細(xì)胞療法在治療多種難治性疾病方面的巨大潛力,也揭示了該領(lǐng)域存在的高成本問(wèn)題。
隨著更多高質(zhì)量隨機(jī)對(duì)照試驗(yàn)結(jié)果的公布和技術(shù)的發(fā)展,我們期待看到更多性價(jià)比高的MSC藥物問(wèn)世,從而更好地滿足未被滿足的醫(yī)療需求,為全球患者帶來(lái)福音。
信息來(lái)源:家干細(xì)胞
免責(zé)說(shuō)明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問(wèn),請(qǐng)隨時(shí)聯(lián)系我。




 掃碼添加官方微信
掃碼添加官方微信