近日,發表于《SAGE Open Med Case Rep》(2026年1月27日)的一項初步臨床研究表明,霧化吸入人臍帶間充質干細胞來源外泌體,有望成為哮喘與慢性阻塞性肺疾病(COPD)的一種新型輔助療法。該回顧性病例報告評估了3例患者接受每周1次、為期5周霧化外泌體治療的安全性與有效性[1]。

結果顯示,治療后患者肺功能多項指標呈現改善趨勢,其中第一秒用力呼氣容積(FEV1)從平均2.59升升至3.4升,用力肺活量(FVC)從2.48升升至3.32升,FEV1/FVC比值也從82.57%提高至92.9%。在炎癥指標方面,C反應蛋白、嗜酸性粒細胞計數等保持穩定,且治療期間未報告任何不良反應,肝腎功能及血液學指標均未見明顯異常。
研究提示,該療法在改善氣流受限、緩解呼吸道癥狀方面具備潛力,且安全性良好,為慢性呼吸系統疾病的無細胞治療提供了初步的臨床依據。
那么,什么是人臍帶間充質干細胞來源的外泌體(hUCMSC-Exo)療法?其相對于傳統干細胞療法的核心優勢體現在哪里?
這種療法代表了再生醫學從“細胞治療”向“無細胞治療”的重要范式轉變。
- 本質:hUCMSC-Exo并非細胞,而是由人臍帶間充質干細胞分泌的、直徑在納米級別的細胞外囊泡。它們可以被視為干細胞天然產生的、高度復雜的“生物活性包裹”或“信號快遞包”。
- 內含物與功能:這些囊泡內富含來源細胞的蛋白質、脂質、信使RNA(mRNA)和尤為關鍵的microRNA等生物活性物質。它們作為細胞間通信的核心媒介,能將上述指令性分子直接傳遞給靶細胞(如受損的肺上皮細胞、免疫細胞),從而遠程調控其行為,實現抗炎、修復等治療目的。
核心優勢(與傳統干細胞移植相比):
- 極高的安全性:從根本上避免了活細胞移植可能帶來的風險,如免疫排斥反應(盡管MSCs免疫原性低,但非零)、細胞在體內不受控增殖或分化的潛在風險(如成瘤性),以及因細胞體積較大可能引發的肺血管栓塞等。
- 卓越的穩定性與可操作性:外泌體更易于標準化生產、長期儲存、質量控制和劑量精確量化,更像一種“現成的生物制劑”,臨床轉化路徑更接近傳統藥物。
- 低倫理爭議:其來源(臍帶)通常被視為醫療廢棄物,獲取過程無創、倫理問題少,且可建立穩定的細胞系進行規模化生產。
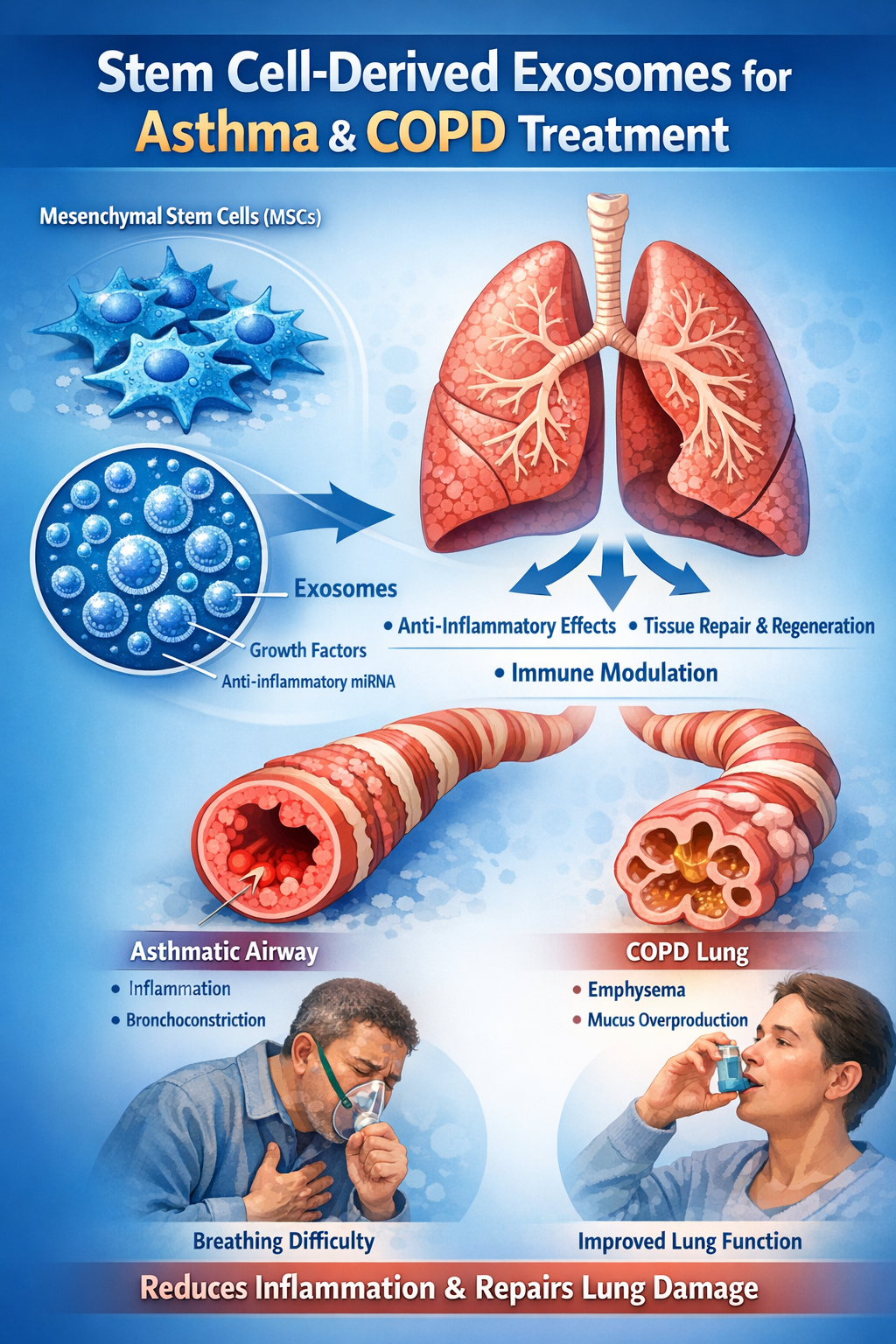
為何霧化吸入hUCMSC-Exo在治療哮喘和COPD等慢性呼吸系統疾病中具有“變革性”潛力?
其潛力建立在“藥物特性”、“疾病病理”與“遞送方式”三者的匹配之上。
- 病理機制的高度針對性:哮喘和COPD的核心病理特征包括“慢性氣道炎癥”、“免疫失衡”和“組織損傷/修復障礙”。hUCMSC-Exo的內容物恰好能針對性調節這些過程。
- 強大的臨床前證據鏈:研究證實,它在動物模型中能抑制過度活化的免疫細胞以減輕氣道炎癥,同時能夠抑制膠原蛋白過度沉積(纖維化),并促進受損的氣道上皮和肺泡細胞修復。
- 霧化吸入遞送方式的“精準”與“高效”:通過霧化直接將藥物遞送至病變的呼吸道和肺泡,實現局部高濃度給藥,生物利用度高,且全身副作用風險極小。同時,霧化吸入作為一種無創、便捷的常規給藥方式,患者依從性好。
hUCMSC-Exo在分子層面是如何發揮治療作用的?其作用機制有何精妙之處?
其作用機制是一個多靶點、協同的精密調控網絡,主要可分為兩大類:
策略一:直接“中和”與“攔截”炎癥風暴(胞外作用):hUCMSC-Exo表面和內部攜帶多種天然的“抗炎分子誘餌”,例如可溶性腫瘤壞死因子受體(sTNFRI/II)、白細胞介素-1受體拮抗劑(IL-1Ra)等。它們能快速結合并中和促炎因子,從上游削弱炎癥級聯反應。
策略二:重編程免疫微環境(胞內作用):外泌體被靶細胞內吞后,其攜帶的microRNA等進入細胞內部,從基因表達層面重塑細胞功能,例如促使促炎的M1型巨噬細胞向抗炎、促修復的M2型轉化,誘導調節性T細胞生成。這不僅抑制了當下炎癥,更將病灶局部的免疫狀態從“攻擊模式”扭轉為“修復模式”。
簡言之,hUCMSC-Exo通過“胞外快速中和”與“胞內長效重編程”的雙重機制,實現了對復雜、慢性氣道炎癥的有效調控。
這項研究怎么做的?方案是什么?主要評估的指標是什么?
這項研究是一項回顧性病例分析,旨在評估霧化人臍帶間充質干細胞來源外泌體對治療3名哮喘及慢性阻塞性肺疾病(COPD)患者的安全性與初步療效。本臨床病例研究納入了三名受試者,平均年齡為59歲(標準差=1.7歲),其中一名女性,兩名男性,他們在2024年至2025年間接受了人臍帶間充質干細胞 (hUCMSC) 來源的外泌體治療(表1)。
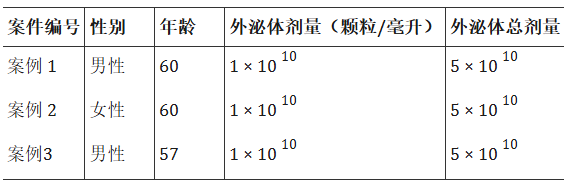
研究方案的核心是一項為期5周的吸入式治療療程。具體而言,由符合良好生產規范(GMP)標準的企業提供的、經過嚴格質量控制(包括粒徑、濃度、無菌性檢測)的外泌體,與生理鹽水混合后,每周一次通過醫用霧化器對患者進行吸入給藥,每次治療持續30分鐘,確保藥物能直接、高效地遞送至肺部靶區。
研究主要通過對比治療前(第0周)與治療后(第6周)的各項指標來評估效果。主要評估指標聚焦于肺功能與系統性炎癥水平,具體包括第一秒用力呼氣容積(FEV1)、用力肺活量(FVC)等肺功能檢查的核心參數,以及反映全身炎癥狀態的C反應蛋白(CRP)水平和全血細胞計數。
次要評估指標則更為廣泛,旨在全面考察癥狀改善與治療安全性。一方面,它評估了患者主觀癥狀的緩解程度,如呼吸困難與胸悶;另一方面,它系統監測了治療對生命體征及主要器官功能的潛在影響,包括心率、血氧飽和度(SpO?),以及代表肝、腎、心肌等器官功能的實驗室指標(如ALT、肌酐、LDH)。這種設計使得研究不僅能初步判斷療效,還能全面評估這種新型療法的臨床安全性。
結果顯示了怎樣的安全性、耐受性和有效性?
根據研究結果,在三名接受治療的患者中,肺功能與臨床癥狀均顯示出積極改善,表2列出了各項參數及其治療前后的數值。通過治療后30天的重復肺功能檢查,關鍵指標如第一秒用力呼氣容積(FEV1)、用力肺活量(FVC)及FEV1/FVC比值較基線水平均有提升。同時,患者自我報告顯示其呼吸道癥狀(如喘息、呼吸困難)得以緩解,急性加重頻率降低,運動耐力也有所提高,從主觀和客觀兩方面證實了該療法的潛在有效性。
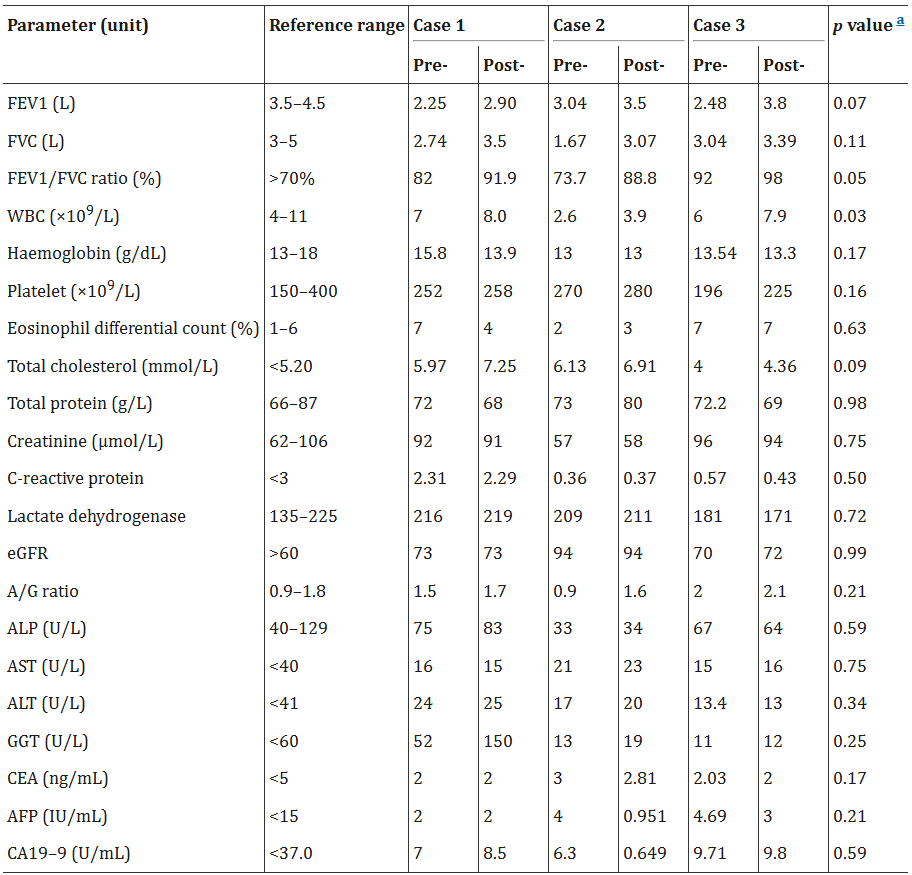
在安全性與耐受性方面,治療表現良好。治療期間所有患者均未報告發熱、胸部不適、過敏反應等不良事件。監測炎癥活動的血清白蛋白/球蛋白比值(A/G比值)在治療前后保持穩定,且癌胚抗原等腫瘤標志物水平均在正常范圍內且無顯著變化,初步表明該療法未引發顯著的全身炎癥反應或潛在腫瘤風險。
有效性通過客觀測量與主觀報告相結合的方式進行評估。研究采用配對t檢驗等統計方法對數據進行分析,核心依據是治療前后肺功能指標的定量比較。此外,將患者反饋的癥狀緩解、生活質量改善等主觀報告結局作為重要補充,共同構成了評估該外泌體療法臨床獲益的完整證據鏈。
該研究得出的主要結論是什么?其意義何在?
本研究的核心結論是:霧化人臍帶間充質干細胞來源外泌體(hUCMSC-Exo)療法,在3例哮喘/慢性阻塞性肺疾病患者中,展現出明確的改善肺功能的潛力,同時具有卓越的全身安全性。其重要性體現在幾個層面:
- 療效初顯:盡管樣本量小,但治療后關鍵肺功能指標呈現一致性的積極變化,為這種無細胞療法在慢性呼吸道疾病中的應用提供了初步的、直接的人體臨床證據。
- 安全性突出:研究對炎癥、血液、肝、腎、代謝及腫瘤標志物進行了系統監測,結果顯示所有指標均未出現具有臨床意義的不良變化,這初步驗證了該療法相較于傳統活細胞治療可能具備的更低系統性風險。
- 機制與臨床的銜接:研究結果(如嗜酸性粒細胞穩定、炎癥指標無惡化)與臨床前研究所揭示的外泌體免疫調節機制相呼應,支持了其作用模式從動物模型到人體患者的可轉化性。
肺功能的具體改善有哪些細節?這些數據如何解讀?
肺功能改善是本研究最突出的療效信號,具體數據及其解讀如下:
- FEV1(反應氣道通暢度):平均值從2.59L提升至3.4L,增幅達31.3%。盡管p=0.07未達到統計學上的嚴格顯著性(通常p<0.05),但其數值增長的臨床意義非常重要,提示患者呼氣初期能排出更多空氣,氣道阻塞減輕。
- FVC(反應肺總容量):從2.48L增至3.32L,增幅33.9%。這表明肺部能夠吸入和呼出更多氣體,肺的擴張和收縮能力增強。
- FEV1/FVC比值(診斷氣流受限的金標準):從82.57%顯著提高至92.9% (p=0.05)。該比值超過90%通常被視為正常或接近正常,這一變化直接表明患者的“阻塞性”病理特征得到了根本性的、具有統計學趨勢的緩解。
- 一致性與支持:所有3名患者的這3項參數均呈現上升趨勢,且與既往使用富含類似抗炎因子(sTNFRI, IL-1Ra等)的外泌體制劑(Exo-d-MAPPS)的臨床報告結果一致,增強了這一發現的可靠性和潛在普適性。
研究如何評估和解讀治療對免疫系統與炎癥狀態的影響?
研究通過多維度指標評估,表明治療產生了積極、可控的免疫調節,而非有害的炎癥激發:
- 輕微的免疫激活信號:白細胞總數從5.2×10?/L升至6.6×10?/L (p=0.03),但數值完全在正常生理范圍內。這更可能解釋為外泌體作為一種生物活性物質,短暫、溫和地激活了免疫監視或修復應答,而非病理性炎癥。
關鍵炎癥通路未受激惹:
- 過敏/嗜酸性粒細胞炎癥:哮喘的關鍵標志物——嗜酸性粒細胞百分比保持穩定(5.33%→4.67%),表明治療沒有加劇過敏性炎癥。這支持了臨床前研究中外泌體能抑制Th2細胞因子(IL-5, IL-13)的發現。
- 全身非特異性炎癥:C反應蛋白水平幾乎無變化,進一步確認治療未引發系統性炎癥反應。
機制關聯:這些臨床發現與討論中提到的機制相符——外泌體攜帶的免疫調節因子(如IL-10, TGF-β, miR-146a)可能促進了免疫細胞從促炎(M1, Th17)向抗炎/修復(M2, Treg)的表型轉化,從而在不抑制整體免疫力的前提下,精準下調了肺部的病理性炎癥。
關于治療的全身安全性,研究提供了哪些詳盡的證據?
研究進行了極其全面的安全性掃查,證據涵蓋多個系統:
- 肝臟安全:所有關鍵肝酶(ALT, AST, ALP, GGT)治療后均在正常范圍內,且波動無統計學意義(如ALT的p=0.34)。這強有力地表明治療未導致肝細胞損傷或膽汁淤積。
- 腎臟安全:肌酐水平和估算的腎小球濾過率(eGFR)在治療前后幾乎完全相同(如肌酐81.67vs81μmol/L),證明腎功能未受任何影響。
- 代謝影響監測:總膽固醇有輕微上升趨勢(p=0.09),雖不顯著,但提示在未來大規模研究中需關注血脂代謝的長期影響。總蛋白水平絕對穩定,說明對全身蛋白質平衡無干擾。
- 血液學安全:血紅蛋白和血小板計數的變化均在正常生理波動范圍內,無貧血、血栓或出血風險跡象。
- 至關重要的腫瘤安全性:癌胚抗原(CEA)、甲胎蛋白(AFP)等腫瘤標志物水平全部保持正常且穩定(如CEA的p=0.17)。這是排除療法潛在促腫瘤風險的關鍵證據,結合外泌體本身無增殖能力的特點,為其長期安全性提供了重要支持。
總體優勢總結:以上所有安全性數據,共同印證了“討論”中指出的理論優勢——基于外泌體的無細胞療法,有效規避了活細胞移植可能面臨的免疫排斥、異常分化和成瘤風險,為其臨床轉化奠定了堅實的安全基礎。
結論
這項回顧性病例系列研究初步證實,霧化吸入人臍帶間充質干細胞來源的外泌體可能對哮喘和COPD患者具有治療益處。肺功能改善、炎癥標志物穩定以及未出現明顯不良反應表明該療法耐受性良好。盡管這些發現令人鼓舞,但仍需開展更大規模的對照研究來證實這些結果并建立標準化的治療方案。
參考資料:
[1]:Yusof B, Foo RQ, Ravichandran M, Sa’ad MA, Tham SK. A case report on nebulized human umbilical cord mesenchymal stem cell-derived exosome therapy for asthma and chronic obstructive pulmonary disease: A preliminary clinical evaluation. SAGE Open Med Case Rep. 2026 Jan 27;14:2050313X251386547. doi: 10.1177/2050313X251386547. PMCID: PMC12855734.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加官方微信
掃碼添加官方微信