系統性紅斑狼瘡(SLE)是一種非常復雜的自身免疫性疾病,患者往往需要長期依賴糖皮質激素和免疫抑制劑來控制病情。但這些傳統治療手段效果有限,副作用又比較明顯,很多人因此陷入長期困擾。
進入2025年,隨著多項重要研究成果的公布以及新技術的不斷應用,干細胞療法正在逐步從實驗階段走向臨床實踐,為全球數百萬患者帶來了新的希望。
本文結合最新的臨床研究進展,對2025年1月至12月干細胞治療系統性紅斑狼瘡的關鍵成果進行梳理,從基礎研究到臨床轉化,全面呈現這一領域的前沿動態和未來發展方向。

2025年1-12月干細胞治療系統性紅斑狼瘡匯總
2025年1月干細胞治療系統性紅斑狼瘡最新臨床進展
2025年1月13日,深圳市北科生物科技有限公司(北科生物)在北京大學人民醫院成功召開了人臍帶間充質干細胞注射液治療中重度系統性紅斑狼瘡(SLE)的Ⅰ/Ⅱ期臨床研究項目啟動會。[1]
該項目已獲得國家藥品監督管理局的批準(批件號:2024LP01052),標志著國內首個針對中重度系統性紅斑狼瘡的干細胞治療注冊臨床研究正式拉開序幕,同時也是國際上少數針對該適應癥采用隨機、雙盲、安慰劑對照臨床試驗之一,對干細胞及適應癥研究具有里程碑式的意義。

項目負責人栗占國教授指出,該療法無需預處理,安全性高,有望為SLE患者提供標準化治療方案。這一試驗的開展不僅填補了國內空白,也為全球SLE治療提供了高質量的循證依據。
2025年2月干細胞治療系統性紅斑狼瘡最新臨床進展
2月初,印度尼西亞三佛齊大學醫學院在國際期刊《生物醫學與轉化研究雜志》上發表了一篇關于《間充質干細胞分泌組在系統性紅斑狼瘡中的免疫調節作用:一項薈萃分析》的研究成果。系統性檢索了PubMed、Embase和Web of Science數據庫中2013年至2024年間發表的關于間充質干細胞治療SLE療效的研究。[2]

本次研究共納入了9項隨機對照試驗(n=485例患者)符合納入標準。分析結果顯示,MSCs療法顯著改善了SLE患者的疾病活動性:SLEDAI評分平均降低0.78,抗雙鏈DNA抗體水平下降0.62,補體C3水平提升0.55。此外,所有患者對MSCs治療耐受性良好,未報告嚴重不良事件。
本薈萃分析表明,MSCS療法對SLE具有顯著的免疫調節作用,可改善疾病活動性和免疫學特征。未來仍需開展更大規模、設計更完善、隨訪期更長的隨機對照試驗來證實這些發現,并評估MSCS治療SLE的長期療效和安全性。
2025年3月干細胞治療系統性紅斑狼瘡最新臨床進展
3月3日,印度尼西亞科研人員在國際期刊《narraj》上發表了一篇關于《臍帶間充質干細胞來源的分泌物作為系統性紅斑狼瘡的潛在治療方法:一項雙盲隨機對照試驗》的研究成果。[3]

研究納入29名女性SLE患者,隨機接受每周一次臍帶間充質干細胞(UCMSC)分泌的蛋白成分治療或安慰劑,持續六周。
結果顯示,與安慰劑組相比,治療組患者的病情活動評分(MEX-SLEDAI)顯著下降,關鍵免疫指標補體C3水平明顯回升,促炎因子IL-6和TNF-α呈下降趨勢,抗dsDNA抗體也有改善趨勢。
值得注意的是,整個治療過程未出現嚴重不良反應,安全性良好。
該研究首次通過雙盲設計驗證了干細胞分泌物在SLE治療中的潛力,為開發非細胞形式的干細胞療法(如條件培養基、外泌體)提供了重要依據。未來需擴大樣本量并延長隨訪時間,進一步明確其長期療效及作用機制,為SLE患者提供更安全、便捷的治療選擇。
2025年4月干細胞治療系統性紅斑狼瘡最新臨床進展
4月初,法國免疫學和移植臨床研究中心牽頭在國際知名期刊《柳葉刀》風濕病學上發表了一篇關于《同種異體臍帶間充質基質細胞治療系統性紅斑狼瘡:一項單中心、開放標簽、劑量遞增、1期研究》的臨床研究成果。[4]

這項歷時近4年的研究(2019.5-2023.3)原本計劃納入干細胞治療系統性紅斑狼瘡(SLE)患者,最終從29名篩選者中入組8人后提前終止招募,且無患者接受1×10?劑量的臍帶間充質基質細胞。入組者中88%為女性,平均年齡35歲,患 SLE平均12年,接受的細胞劑量為每公斤2×10?至 4×10?個。
治療后短期觀察發現2人出現輕微不良反應(如發熱),長期隨訪(約1年)中1人病情復發,但未發現與治療直接相關的嚴重問題。
這項小規模臨床試驗表明,臍帶間充質干細胞治療系統性紅斑狼瘡在短期內安全性較高,且長期隨訪中未發現與治療直接相關的嚴重問題,為患者提供了潛在的新療法。
4月29日,《健康報》第003版以《心有鴻鵠志 領跑克頑疾》為題,聚焦南京鼓樓醫院風濕免疫醫學中心主任孫凌云教授團隊在自身免疫性疾病治療領域的重大突破。
系統性紅斑狼瘡(SLE)作為曾令全球醫學界束手無策的“不死的癌癥”,因中國原創的異體間充質干細胞療法迎來歷史性轉折。該團隊歷時30余年科研攻關,首創“間充質干細胞免疫調控技術體系”,成功救治全球2800余例重癥患者。這一技術不僅榮獲國家技術發明獎二等獎,更將治療有效率提升至60%,5年死亡率從45%顯著降至16%,兩項干細胞新藥也已進入Ⅱ期臨床試驗沖刺階段。

以2007年21歲的患者珊珊(化名)為例,她因紅斑狼瘡導致全身潰爛、股骨頭壞死瀕臨絕望,成為全球首例接受異體間充質干細胞移植的患者。治療后,她的月經恢復、血液指標逐步正常,盡管因早期副作用行動不便,但十幾年過去紅斑狼瘡病情再未復發,成為這項技術治愈力的生動見證。
目前,相關新藥研究正穩步推進。孫凌云教授表示:“從一期臨床結果來看,該療法對狼瘡性腎炎和系統性硬化癥安全可靠,未出現嚴重不良反應。”這一成果不僅為重癥自身免疫性疾病患者帶來曙光,更彰顯了中國在干細胞治療領域的國際領先地位。
2025年5月干細胞治療系統性紅斑狼瘡最新臨床進展
經中南大學湘雅醫院臨床醫學倫理審查委員會批準,“人臍帶間充質干細胞注射液(hUCMSCs)治療中重度系統性紅斑狼瘡患者的安全性、有效性、藥效學和免疫原性的I/II期臨床研究”(簡稱“BK-SLE-I/01”項目)正式啟動,標志著我國在干細胞治療自身免疫性疾病領域邁出重要一步。[5]
來自貴州的小王(化名)是首位參與該項目的研究參與者。她長期受系統性紅斑狼瘡困擾,多次嘗試傳統治療方案均未取得顯著療效。2025年4月,小王在湘雅醫院就診時,由項目主要研究者趙洪軍副教授團隊評估后,充分了解研究獲益與風險,并完成知情同意、篩選及入組流程,成為全國首例入組患者。

與此同時,另一位來自岳陽平江的患者小湛(化名)也因系統性紅斑狼瘡長期治療無效,選擇參與“BK-SLE-I/01”項目。在趙洪軍副教授團隊的指導下,小湛順利完成治療方案,并于5月底收到研究團隊關于治療進展的反饋。
“BK-SLE-I/01”項目的順利推進,不僅為中重度系統性紅斑狼瘡患者提供了新的治療選擇,也驗證了干細胞療法在調節免疫、修復組織方面的潛力。隨著更多患者入組和數據積累,該研究有望為全球自身免疫性疾病的治療提供中國方案,推動再生醫學領域的創新發展。

2025年7月干細胞治療系統性紅斑狼瘡最新臨床進展
7月29日,《化學工程雜志》上發表了一篇名為《載有hUC-MSCs外泌體的水凝膠用于系統性紅斑狼瘡傷口治療》的研究成果。[6]

研究結果表明,hUC-MSCs Exos能夠增強成纖維細胞的生物學功能,包括增殖、遷移以及體外培養的HUVEC遷移和血管生成。
為了優化hUC-MSCs Exos的臨床應用療效,我們選擇了經臨床驗證的水凝膠作為遞送載體,該載體具有有效的緩釋能力。作為細胞外基質的天然成分,HA具有優異的生物相容性,最大限度地減少了狼瘡的炎癥,從而促進傷口愈合。
因此,我們相信,我們的hUC-MSCs外泌體遞送系統可以作為一個穩定高效的MSC治療平臺,在系統性紅斑狼瘡(SLE)傷口治療中展現出巨大的潛力。
2025年8月干細胞治療系統性紅斑狼瘡最新臨床進展
8月5日,南京鼓樓醫院牽頭在《英國醫學雜志》上發表了一篇名為《間充質干細胞通過CTGF/FAK信號抑制系統性紅斑狼瘡中的纖維化,從而改善卵巢功能》的研究成果。[7]
本研究探討臍帶間充質干細胞(UC-MSCs)在狼瘡小鼠模型中通過抑制纖維化來改善卵巢功能損傷、恢復卵巢功能的療效。

研究結果表明,UC-MSC移植顯著下調促炎性細胞因子(Tnf-α、Il-1β)和纖維化標志物(Ctgf、α-Sma)的表達,同時上調關鍵激素受體(Amh、Esr1、Esr2 )的表達。
此外,還觀察到CD3+/CD4+T細胞浸潤、C3補體沉積和IgG水平降低,同時調節性T細胞增加。進一步分析顯示,MSC移植后,原代卵巢GC中的纖維化標志物和FAK-Tyr576/577磷酸化受到顯著抑制。
體外實驗表明,重組CTGF可促進人GC系KGN中的纖維化。相反,MSC治療抑制了磷酸化的FAK-Tyr576/577并下調了膠原蛋白1和α-SMA的表達,這表明UC-MSC通過抑制FAK-Tyr576/577磷酸化來減輕卵巢纖維化。
本研究表明,UC-MSC 治療通過調節 CTGF/FAK-Tyr576/577 磷酸化通路改善了狼瘡小鼠的卵巢功能障礙并減輕了卵巢纖維化。
2025年9月干細胞治療系統性紅斑狼瘡最新臨床進展
9月9日,IRCCS圣拉斐爾醫院牽頭在國際知名期刊《nature》上發表了一篇名為《造血干細胞移植和CAR-T療法治療血液系統疾病、實體瘤和免疫系統疾病的適應癥:2025年歐洲骨髓移植協會(EBMT)實踐指南》的報告。[8]
歐洲骨髓移植協會(EBMT)基于臨床實踐和科研進展,定期更新造血干細胞移植(HCT)適應癥指南。本報告是第九版,旨在幫助各成員國和醫療機構依據當前證據合理使用HCT。指南內容不僅考慮疾病本身風險和 HCT 手術風險,也關注替代療法(包括新興細胞療法)的可及性,強調以患者利益為核心進行綜合評估。

在多種自身免疫性疾病的治療中,自體造血干細胞移植(auto-HCT)已被證明具有潛在療效。其中,對于系統性紅斑狼瘡(SLE),已有研究證據支持在經過嚴格篩選后使用自體干細胞移植進行治療。
現有文獻表明,自體造血干細胞移植能夠改善部分難治性SLE患者的疾病狀況,尤其在傳統免疫抑制治療無效的情況下,為患者提供一種“免疫系統重置”的治療機會。
此外,隨著醫療中心在患者篩選、預處理方式和配套支持治療方面經驗的積累,自體干細胞移植在自身免疫病中的成功率逐步提高,治療風險得到相對控制,進一步增強了其作為治療SLE的潛在選擇價值。
2025年10月干細胞治療系統性紅斑狼瘡最新臨床進展
10月3日,我國科研人員在《Mol Med Rep》期刊上發表了一篇名為《誘導多能干細胞在自身免疫性疾病研究和治療中的應用潛力(綜述)》的研究成果。[9]

研究指出,誘導多能干細胞(iPSCs)在自身免疫性疾病中展現出顯著的治療潛力。它們能夠通過調節異常免疫反應、抑制炎癥反應以及修復受損組織,從而改善腎臟、心臟、血液系統等多個器官的功能。
與傳統的免疫抑制治療相比,干細胞療法不僅具有更強的個性化和再生能力,還可在緩解癥狀的同時減輕器官損傷,為系統性紅斑狼瘡(SLE)等自身免疫性疾病患者帶來新的治療希望。
2025年12月干細胞治療系統性紅斑狼瘡最新臨床進展
12月24日,深圳恩瑞愷諾生物技術有限公司啟動了一項KN5501細胞注射液治療中重度難治性系統性紅斑狼瘡(SLE)的Ⅰ期臨床試驗(臨床試驗登記號:CTR20255045)。[10]
該研究旨在評估KN5501的安全性、耐受性,確定最大耐受劑量(MTD)和Ⅱ期推薦劑量(RP2D),并探索其藥代動力學(PK)和藥效動力學(PD)特征。
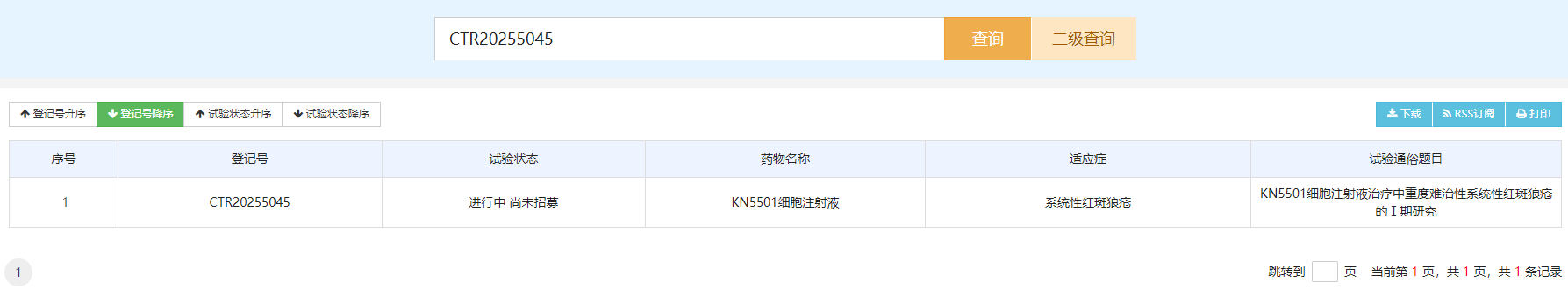
該試驗的主要終點包括劑量限制性毒性(DLT)、不良事件(AE)、體格檢查、生命體征、實驗室指標及心電圖變化;次要終點包括CAR?NK細胞水平、CD19?B細胞計數、不同緩解標準的達成率、SLEDAI-2000和ssPGA評分變化、患者報告結局(PRO)量表、抗CAR抗體水平及病毒安全性指標。
2025年干細胞治療系統性紅斑狼瘡最新臨床進展總結
綜上所述,2025年干細胞治療系統性紅斑狼瘡(SLE)的全球進展表明,干細胞療法正從實驗室走向臨床實踐,成為傳統治療無效患者的潛在新選擇。通過多項隨機對照試驗和薈萃分析,間充質干細胞(MSCs)在降低疾病活動性、改善免疫紊亂(如補體水平、抗體滴度)及安全性方面展現出顯著優勢。
尤其值得關注的是,中國在技術體系創新、新藥研發及臨床轉化方面走在最前列,為全球自身免疫性疾病治療提供了“中國方案”。
未來需進一步擴大樣本量、延長隨訪周期,明確最佳劑量及作用機制,推動干細胞療法標準化、規范化,最終惠及更多SLE患者,重塑免疫疾病治療格局。
干細胞治療系統性紅斑狼瘡的臨床研究項目進展
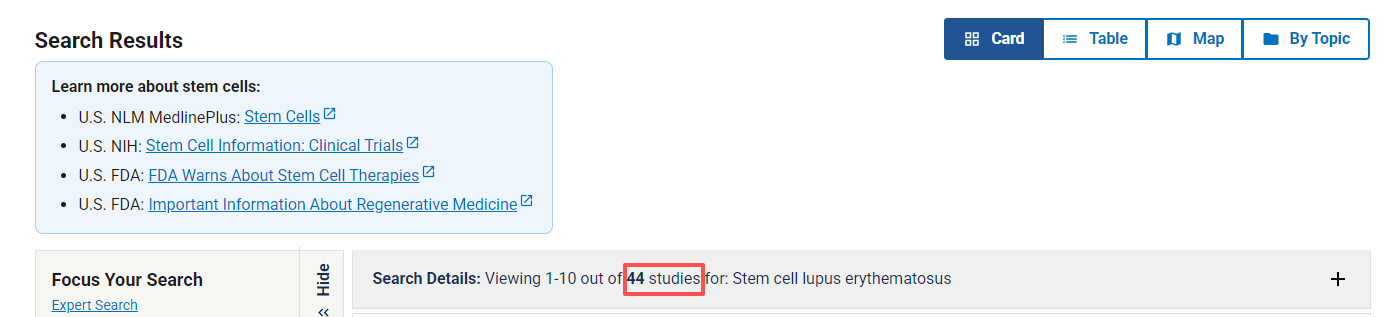
截止2025年12月31日,在美國國立衛生研究院的最大臨床試驗注冊庫clinicaltrials.gov網站上注冊的有關干細胞治療系統性紅斑狼瘡的臨床研究項目達到44項。
結語
2025年干細胞治療系統性紅斑狼瘡進入了一個更實際、更接近臨床應用的階段。越來越多的隨機對照試驗和薈萃分析顯示,間充質干細胞(MSCs)在降低疾病活動度、調整免疫失衡并且總體安全性方面都有可觀表現,為那些對傳統藥物反應不佳的患者帶來了新的選擇。
中國在這條路上動作很快:從技術體系創新到新藥研發,再到把成果推向臨床轉化,相關團隊和試驗數量都在增加,“中國方案”在國際上正逐步被看到和認可。
當然,要真正把這種治療變成日常可及的手段,還需要解決幾個問題:擴大樣本量、把作用機制說清楚、以及把細胞制備和給藥流程做到標準化。一旦這些環節成熟,干細胞療法很可能會重塑部分SLE的治療路線,讓更多患者真正受益。
參考資料:
[1]https://bydrug.pharmcube.com/news/detail/5ad244ef47698b032769c6b2c7438f59
[2]Narisa Felinka Kusuma, & Nova Kurniati. (2025). Immunomodulatory Effects of Mesenchymal Stem Cell Secretome in Systemic Lupus Erythematosus: A Meta-Analysis. Bioscientia Medicina : Journal of Biomedicine and Translational Research, 9(4), 6911-6924. https://doi.org/10.37275/bsm.v9i4.1244
[3]Nurudhin A, Werdiningsih Y, Sunarso I, Marwanta S, Damayani A, Prabowo NA, Affandi A, Gazali I, Safitri AS, Sidarta BR. Umbilical cord mesenchymal stem cell-derived secretome as a potential treatment for systemic lupus erythematosus: A double-blind randomized controlled trial. Narra J. 2025 Apr;5(1):e1799. doi: 10.52225/narra.v5i1.1799. Epub 2025 Mar 3. PMID: 40352183; PMCID: PMC12059846.
[4]Farge D, Biard L, Weil B, Girault V, Lansiaux P, Munia I, Loisel S, Charles C, Saout J, Resche-Rigon M, Korganow AS, Beuvon C, Pugnet G, Cacciatore C, Abisror N, Taupin JL, Cras A, Lowdell MW, Tarte K. Allogeneic umbilical cord-derived mesenchymal stromal cells as treatment for systemic lupus erythematosus: a single-centre, open-label, dose-escalation, phase 1 study. Lancet Rheumatol. 2025 Apr;7(4):e261-e273. doi: 10.1016/S2665-9913(24)00298-4. Epub 2024 Dec 17. PMID: 39706212.
[5]https://mp.weixin.qq.com/s/bu8qpjMvi8hWIwZGfSZDFA?poc_token=HDTXkWijr9ta3pwzx5lSvZyjPgSJoGee1-ziP99g
[6]Defang Meng, Danqing Huang, Xiaoquan Wei, Min Nie, Xiulan Zheng, Yuanjin Zhao, Lingyun Sun,
hUC-MSCs exosomes-loaded hydrogels for systemic lupus erythematosus wound treatment,Chemical Engineering Journal,Volume 521,2025,166491,ISSN 1385-8947,https://doi.org/10.1016/j.cej.2025.166491.[7]Haiwei Zhang, Hui Yang, Yingyi Wu, Yirui Shi, Min Xu, Yueyang Zhang, Hongwei Chen, Lingyun Sun – Mesenchymal stem cells improve ovarian function by suppressing fibrosis through CTGF/FAK signalling in systemic lupus erythematosus: Lupus Science & Medicine 2025;12:e001468.
[8]Greco, R., Ruggeri, A., McLornan, D.P. et al. Indications for haematopoietic cell transplantation and CAR-T for haematological diseases, solid tumours and immune disorders: 2025 EBMT practice recommendations. Bone Marrow Transplant (2025). https://doi.org/10.1038/s41409-025-02701-3
[9]Ye Z, Zhao H, Ye X. Application potential of induced pluripotent stem cells in the research and treatment of autoimmune diseases (Review). Mol Med Rep. 2025 Dec;32(6):333. doi: 10.3892/mmr.2025.13698. Epub 2025 Oct 3. PMID: 41041834; PMCID: PMC12511849.
[10]https://www.163.com/dy/article/KHIJ0CLT05568W0A.html
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加官方微信
掃碼添加官方微信