神經(jīng)退行性疾病(NDs)嚴(yán)重影響患者的生活質(zhì)量,而有效的治療方法仍然有限。由于治療重點(diǎn)在于緩解癥狀,因此通常忽略了問題的根本原因。干細(xì)胞具有自我更新和分化成多種細(xì)胞系的能力,展現(xiàn)出巨大的潛力,使其成為再生療法(尤其是神經(jīng)系統(tǒng)疾病)的理想候選者。
間充質(zhì)干細(xì)胞療法在4大神經(jīng)退行性疾病中的應(yīng)用:機(jī)制、臨床進(jìn)展與未來展望
2026年1月13日,《Biology and Life Sciences》發(fā)表的一篇研究綜述,為間充質(zhì)干細(xì)胞治療神經(jīng)系統(tǒng)疾病提供了有力證據(jù)。該綜述指出,間充質(zhì)干細(xì)胞及其衍生物對多種神經(jīng)退行性疾病具有疾病修飾作用。在阿爾茨海默病(AD)、帕金森病(PD)、亨廷頓病(HD)和肌萎縮側(cè)索硬化癥(ALS)的臨床前研究中,一致觀察到行為學(xué)改善、神經(jīng)炎癥減輕以及神經(jīng)保護(hù)效應(yīng)。這些作用主要源自MSCs的旁分泌信號,而非直接的細(xì)胞替代[1]。
迄今為止的臨床研究一致支持基于MSCs療法的安全性和可行性,但療效信號仍然有限、異質(zhì)性較高且主要為短期療效,這凸顯了開展更大規(guī)模、控制良好的臨床試驗(yàn)的必要性。
間充質(zhì)干細(xì)胞的顯著優(yōu)勢與治療基礎(chǔ)
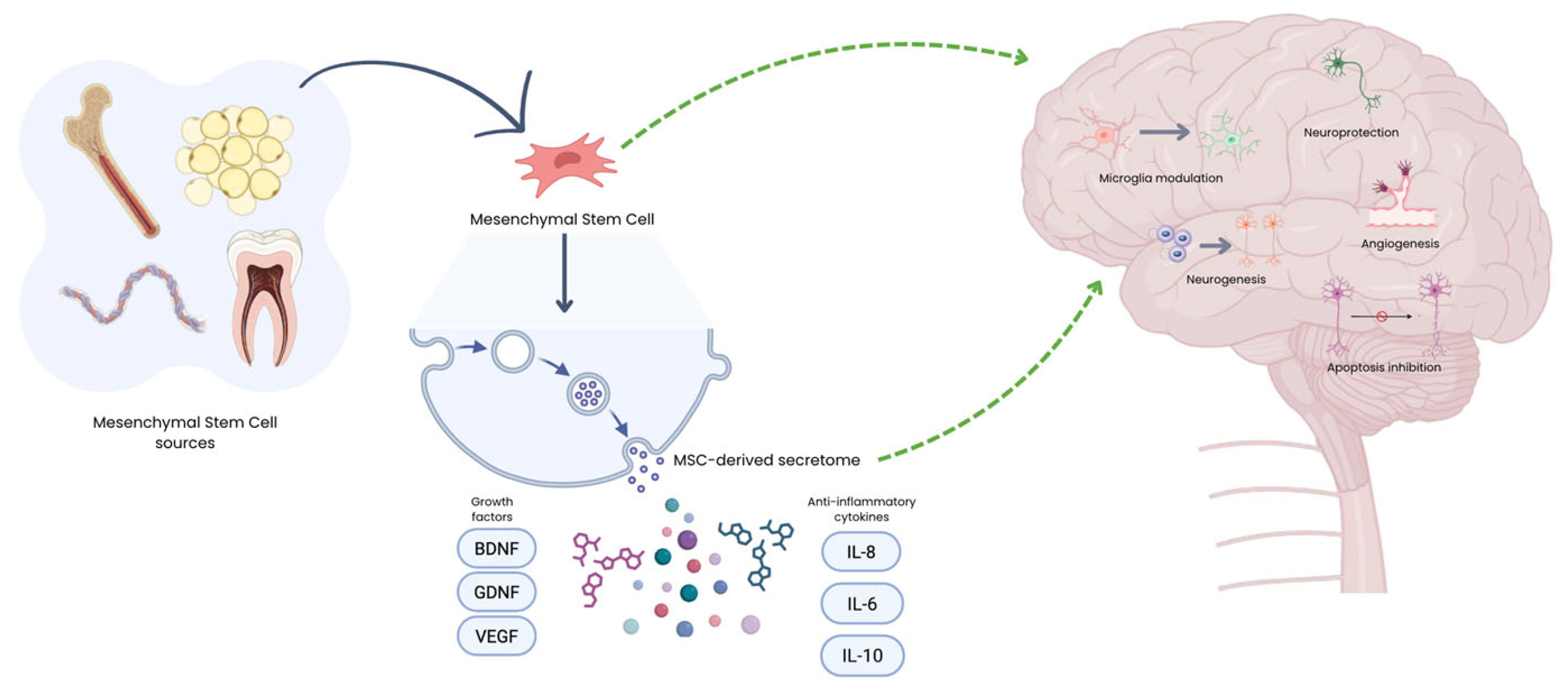
間充質(zhì)干細(xì)胞(MSCs)的核心治療價(jià)值在于其三大優(yōu)勢:來源廣泛且倫理爭議小(可從骨髓、脂肪、臍帶、牙髓等多種組織輕松獲取)、低免疫原性(允許使用異體來源而無需嚴(yán)格配型,極大降低了臨床應(yīng)用門檻)以及作用機(jī)制安全高效(圖1)。
其治療作用主要不依賴直接分化替代受損細(xì)胞,而是通過強(qiáng)大的旁分泌效應(yīng)來實(shí)現(xiàn),即分泌一系列生物活性物質(zhì)(統(tǒng)稱“分泌組”),包括細(xì)胞因子(如抗炎因子IL-10)、生長因子(如促進(jìn)神經(jīng)生長的BDNF)以及包裹了蛋白質(zhì)、mRNA和微RNA(miRNA)的細(xì)胞外囊泡。這些物質(zhì)共同起到調(diào)節(jié)免疫、抑制炎癥、促進(jìn)血管新生、保護(hù)現(xiàn)存細(xì)胞并刺激內(nèi)源性修復(fù)的關(guān)鍵作用(圖1)。
核心治療載體——細(xì)胞外囊泡(EVs)及其靶向遞送優(yōu)勢
在MSCs的分泌組中,細(xì)胞外囊泡(EVs) 因其獨(dú)特的納米級囊泡結(jié)構(gòu),已成為最具前景的“無細(xì)胞”治療工具。EVs的核心優(yōu)勢在于其天然的生物遞送能力:它能夠攜帶母細(xì)胞(MSCs)的治療性物質(zhì),并有效地穿越體內(nèi)屏障,尤其是難以逾越的血腦屏障,從而將藥物精準(zhǔn)遞送至大腦等中樞神經(jīng)系統(tǒng)病變部位,解決了傳統(tǒng)大分子藥物難以入腦的難題(圖1)。
然而,EVs的遞送效率并非一成不變,它受到囊泡本身物理特性(如大小、表面電荷)、生化組成(取決于MSCs的來源和培養(yǎng)條件)以及給藥途徑等多種因素的復(fù)雜影響,其精確作用機(jī)制仍是當(dāng)前研究的前沿。
在神經(jīng)退行性疾病中的具體應(yīng)用機(jī)制與前景
基于上述機(jī)制,MSCs及其EVs在對抗神經(jīng)退行性疾病中展現(xiàn)出多方面的治療潛力,其作用因疾病病理特點(diǎn)而有所側(cè)重:
- 在阿爾茨海默病(AD)中,主要通過減輕腦內(nèi)慢性神經(jīng)炎癥和提供神經(jīng)營養(yǎng)支持來保護(hù)神經(jīng)元、延緩認(rèn)知衰退;
- 在帕金森病(PD)中,重點(diǎn)在于釋放神經(jīng)營養(yǎng)因子(如GDNF),支持殘存的多巴胺能神經(jīng)元存活并改善其功能;
- 在亨廷頓病(HD)等疾病中,則能激活抗凋亡、抗氧化和神經(jīng)保護(hù)通路。
綜上所述,MSCs及其衍生物(尤其是EVs)集多靶點(diǎn)治療、高安全性、良好遞送潛力及易規(guī)模化生產(chǎn)等優(yōu)點(diǎn)于一身,被視為開發(fā)下一代神經(jīng)退行性疾病療法極具競爭力的候選策略。
下文將根據(jù)現(xiàn)有文獻(xiàn)數(shù)據(jù),系統(tǒng)討論MSC療法在治療神經(jīng)退行性疾病中的研究進(jìn)展、安全性、有效性及相關(guān)不良事件。
間充質(zhì)干細(xì)胞針對特定神經(jīng)系統(tǒng)疾病的療法
由于干細(xì)胞具有自我更新、自我復(fù)制、再生和分化能力,最近的研究致力于尋找利用干細(xì)胞治療神經(jīng)退行性疾病的有效治療方案。
01、間充質(zhì)干細(xì)胞與阿爾茨海默病(AD)
阿爾茨海默病(AD)是神經(jīng)退行性疾病中最常見的類型之一,主要影響老年人群。臨床上,AD與癡呆癥相關(guān),其特征是進(jìn)行性記憶喪失和一個(gè)或多個(gè)認(rèn)知領(lǐng)域的損害。退行性變主要影響海馬和皮質(zhì)神經(jīng)元,包括谷氨酸能和膽堿能神經(jīng)元群,導(dǎo)致記憶喪失和認(rèn)知能力下降(圖2) 。

阿爾茨海默病的核心病理機(jī)制——一個(gè)多層次的惡性循環(huán)
阿爾茨海默病的病理核心是β-淀粉樣蛋白(Aβ)和tau蛋白的異常積累,它們通過兩種主要形式造成損害。
第一,不溶性沉積物:Aβ在神經(jīng)元外形成“老年斑”,tau蛋白在神經(jīng)元內(nèi)形成“神經(jīng)原纖維纏結(jié)”,這些固態(tài)結(jié)構(gòu)物理性地破壞突觸連接,阻礙神經(jīng)信號傳遞。
第二,可溶性寡聚體:這些微小、可擴(kuò)散的Aβ和tau寡聚體毒性更強(qiáng),能直接嵌入神經(jīng)元膜,破壞其完整性,干擾線粒體功能,并異常影響神經(jīng)遞質(zhì)釋放。
關(guān)鍵的是,這兩種形式共同觸發(fā)了一個(gè)自我強(qiáng)化的“炎癥循環(huán)”:它們被大腦的免疫細(xì)胞(小膠質(zhì)細(xì)胞和星形膠質(zhì)細(xì)胞)識別,導(dǎo)致其持續(xù)過度激活,釋放大量炎癥因子和神經(jīng)毒性物質(zhì),這種慢性神經(jīng)炎癥反過來又加速了神經(jīng)元損傷和更多病理性蛋白的生成,形成了驅(qū)動疾病進(jìn)展的核心惡性循環(huán)。
傳統(tǒng)療法的困境與間充質(zhì)干細(xì)胞治療的多靶點(diǎn)新策略
針對上述核心病理,傳統(tǒng)的“單一靶點(diǎn)”療法(如直接清除Aβ或tau蛋白的抗體藥物)在大型臨床試驗(yàn)中均告失敗,凸顯了僅干預(yù)疾病鏈條中一個(gè)環(huán)節(jié)的局限性。因此,研究轉(zhuǎn)向了具有多靶點(diǎn)、多功能特性的間充質(zhì)干細(xì)胞(MSCs)及其衍生物(如外泌體)。
臨床前研究(動物實(shí)驗(yàn))清楚地揭示了其作用機(jī)制
它們并非直接“替換”神經(jīng)元,而是作為一個(gè)生物反應(yīng)調(diào)節(jié)系統(tǒng),通過分泌多種活性因子,同時(shí)執(zhí)行“清除”(促進(jìn)Aβ降解)、“滅火”(抑制小膠質(zhì)細(xì)胞過度活化,減輕神經(jīng)炎癥)、“修復(fù)”(提供神經(jīng)營養(yǎng)支持,保護(hù)突觸功能)和“調(diào)節(jié)”(改善細(xì)胞自噬與凋亡平衡) 等多重任務(wù),從而從多個(gè)環(huán)節(jié)上打破上述的病理惡性循環(huán)。
臨床轉(zhuǎn)化現(xiàn)狀——從明確的有效性到初步的安全性,未來挑戰(zhàn)明確
目前,MSCs治療AD的轉(zhuǎn)化醫(yī)學(xué)證據(jù)呈現(xiàn)清晰的兩個(gè)階段。在臨床前階段,證據(jù)高度一致且積極,多種動物模型均證實(shí)MSCs能顯著改善認(rèn)知并減輕核心病理。
然而,在臨床階段,當(dāng)前已完成和進(jìn)行中的早期試驗(yàn)(I/II期)主要核心結(jié)論是證明了多種給藥途徑(如腦室內(nèi)注射、鼻內(nèi)給藥)的安全性、可行性和良好耐受性。在療效方面,僅在一些探索性分析中觀察到了令人鼓舞的初步跡象,如特定劑量組出現(xiàn)認(rèn)知改善減緩、海馬體萎縮減慢等。
因此,結(jié)論非常明確:MSCs療法已成功跨越了臨床轉(zhuǎn)化的第一道關(guān)卡(安全性),但其確鑿的臨床療效尚未得到大規(guī)模驗(yàn)證,必須通過設(shè)計(jì)更嚴(yán)謹(jǐn)、規(guī)模更大、隨訪期更長的II/III期隨機(jī)對照試驗(yàn)來最終確定其治療價(jià)值。
02、間充質(zhì)干細(xì)胞治療帕金森病(PD)
帕金森病的核心病理與診斷困境
帕金森病(PD)是第二常見的神經(jīng)退行性疾病,其核心病理生理機(jī)制是錯(cuò)誤折疊的α-突觸核蛋白在神經(jīng)元內(nèi)異常積聚,形成路易體和路易神經(jīng)突。這導(dǎo)致以黑質(zhì)紋狀體通路多巴胺能神經(jīng)元選擇性喪失,進(jìn)而引發(fā)運(yùn)動障礙。
值得注意的是,α-突觸核蛋白病理在中樞神經(jīng)系統(tǒng)內(nèi)分布廣泛,使得PD具有高度異質(zhì)性。目前臨床診斷僅為“可能”PD,確診仍需死后腦組織病理檢查,這凸顯了該蛋白在發(fā)病中的中心地位及當(dāng)前診斷手段的局限。
MSCs通過分泌組發(fā)揮多靶點(diǎn)疾病修飾作用的臨床前證據(jù)
臨床前研究一致表明,間充質(zhì)干細(xì)胞(MSCs)對PD的治療作用主要依賴其旁分泌功能,而非細(xì)胞直接替代。其分泌組(含神經(jīng)營養(yǎng)因子和細(xì)胞外囊泡EVs)能發(fā)揮多靶點(diǎn)疾病修飾作用:
- 1)對抗核心病理:抑制α-突觸核蛋白的異常聚集,降低其水平;
- 2)神經(jīng)保護(hù)與修復(fù):支持多巴胺能神經(jīng)元存活,保護(hù)黑質(zhì)和紋狀體神經(jīng)元;
- 3)免疫調(diào)節(jié):調(diào)節(jié)小膠質(zhì)細(xì)胞的過度激活,減輕神經(jīng)炎癥。在多種PD動物模型(毒素誘導(dǎo)或α-突觸核蛋白過表達(dá))中,MSC-EV治療能持續(xù)改善運(yùn)動功能、降低炎癥因子水平,且療效可維持?jǐn)?shù)周至數(shù)月,為臨床應(yīng)用提供了堅(jiān)實(shí)的機(jī)制與療效基礎(chǔ)。
早期臨床試驗(yàn)證實(shí)安全性并提示潛在療效趨勢
早期臨床研究(多為I/II期試驗(yàn))探索了不同來源(骨髓、脂肪)和不同途徑(靜脈、鼻內(nèi)、腦內(nèi)/動脈內(nèi)注射)的MSC移植。綜合現(xiàn)有數(shù)據(jù),結(jié)論明確分為兩層:
第一,安全性得到廣泛證實(shí)——無論是自體還是異體MSCs,多種給藥方式均表現(xiàn)出良好的安全性和耐受性,僅報(bào)告輕微或短暫的不良事件,未發(fā)現(xiàn)免疫排斥、致瘤性或MRI異常等嚴(yán)重問題。
第二,療效呈現(xiàn)積極但初步的趨勢——多項(xiàng)試驗(yàn)報(bào)告了患者運(yùn)動癥狀(UPDRS評分)的短期改善,部分研究還觀察到左旋多巴用量減少或病情穩(wěn)定。然而,這些試驗(yàn)大多樣本量有限,缺乏長期隨訪和嚴(yán)格的對照組,因此目前證據(jù)主要確立了MSC療法的安全性,其確切的臨床療效仍需通過大規(guī)模、隨機(jī)雙盲的III期臨床試驗(yàn)來最終驗(yàn)證。
03、間充質(zhì)干細(xì)胞治療亨廷頓舞蹈癥(HD)
亨廷頓舞蹈癥的復(fù)雜病理機(jī)制與MSCs的間接治療策略
亨廷頓舞蹈癥是一種由亨廷頓基因CAG重復(fù)異常擴(kuò)增導(dǎo)致的常染色體顯性遺傳病,致病根源是神經(jīng)毒性的突變型亨廷頓蛋白。該病主要引起紋狀體GABA能神經(jīng)元進(jìn)行性變性,病理生理涉及興奮性毒性、線粒體功能障礙、氧化應(yīng)激、神經(jīng)營養(yǎng)因子缺乏及慢性神經(jīng)炎癥等多重交織的通路。
當(dāng)前MSCs治療策略并非直接糾正遺傳缺陷,而是旨在全面干預(yù)這些下游的共通致病通路,以對抗神經(jīng)退行性變。
臨床前研究的積極證據(jù)與明確的旁分泌作用機(jī)制
大量臨床前研究(超過15項(xiàng)嚙齒動物模型實(shí)驗(yàn))一致表明,移植MSCs(如骨髓或牙髓來源)能帶來顯著的功能和結(jié)構(gòu)性改善。這些益處包括:增加紋狀體體積、減少腦室擴(kuò)大、以及顯著改善運(yùn)動協(xié)調(diào)性等行為學(xué)指標(biāo),但對認(rèn)知功能的改善作用有限。
在機(jī)制上,MSCs主要通過旁分泌信號發(fā)揮作用,而非直接分化為神經(jīng)元。其分泌的神經(jīng)營養(yǎng)因子(特別是腦源性神經(jīng)營養(yǎng)因子BDNF)能上調(diào)內(nèi)源性支持,同時(shí)有效抑制細(xì)胞凋亡、調(diào)節(jié)小膠質(zhì)細(xì)胞活性以減輕神經(jīng)炎癥。
為進(jìn)一步增強(qiáng)療效,基因工程改造的MSCs(如過表達(dá)BDNF的MSC/BDNF) 已顯示出更強(qiáng)大的效果,包括更顯著的神經(jīng)保護(hù)作用和延長模型動物生存期。此外,鼻內(nèi)給藥作為一種非侵入性方式,已被證實(shí)能將MSCs有效靶向遞送至紋狀體,具有重要的轉(zhuǎn)化應(yīng)用前景。
臨床轉(zhuǎn)化處于早期階段,安全性與初步探索并行
目前,MSCs治療HD的臨床轉(zhuǎn)化仍處于初步探索階段,人體數(shù)據(jù)非常有限。現(xiàn)有的早期研究主要聚焦于兩個(gè)方面:
- 一是為后續(xù)細(xì)胞治療試驗(yàn)奠定基礎(chǔ),如PRE-CELL研究旨在確定合適的臨床和影像學(xué)終點(diǎn);
- 二是評估初步的安全性與可行性,例如巴西正在進(jìn)行的試驗(yàn)探索重復(fù)全身輸注MSCs的長期安全性及潛在的神經(jīng)保護(hù)作用。
總體而言,現(xiàn)有證據(jù)表明該療法具有良好的前景和安全性,但在臨床上尚無確鑿的療效結(jié)論。未來方向,特別是利用工程化MSCs進(jìn)行神經(jīng)營養(yǎng)因子靶向遞送的策略,正在成為頗具潛力的重點(diǎn)研究領(lǐng)域,但其最終治療價(jià)值有待嚴(yán)格設(shè)計(jì)的臨床試驗(yàn)驗(yàn)證。
04、間充質(zhì)干細(xì)胞治療肌萎縮側(cè)索硬化癥(ALS)
肌萎縮側(cè)索硬化癥(ALS)的核心特征與復(fù)雜的致病網(wǎng)絡(luò)
肌萎縮側(cè)索硬化癥是一種致命的進(jìn)行性神經(jīng)退行性疾病,核心病理是控制隨意肌的運(yùn)動神經(jīng)元選擇性喪失。約90%病例為散發(fā)性。其病因不明,涉及一個(gè)多因素交織的致病網(wǎng)絡(luò),包括蛋白質(zhì)異常聚集、RNA代謝失調(diào)、興奮性毒性、氧化應(yīng)激、線粒體功能障礙及慢性神經(jīng)炎癥等,共同導(dǎo)致運(yùn)動神經(jīng)元死亡,臨床表現(xiàn)為進(jìn)行性肌無力、萎縮、延髓麻痹及最終呼吸衰竭。
MSCs通過旁分泌機(jī)制在臨床前研究中展現(xiàn)多靶點(diǎn)神經(jīng)保護(hù)作用
臨床前研究(如SOD1突變小鼠模型)的系統(tǒng)評價(jià)表明,間充質(zhì)干細(xì)胞移植能顯著延緩疾病發(fā)病、減緩進(jìn)展并延長生存期。其治療益處主要源于旁分泌作用,而非細(xì)胞替代。
MSCs分泌的多種神經(jīng)營養(yǎng)因子(如BDNF、GDNF、VEGF)和抗炎細(xì)胞因子,共同發(fā)揮多靶點(diǎn)保護(hù)效應(yīng):
- 1)直接營養(yǎng)支持:增強(qiáng)運(yùn)動神經(jīng)元存活能力;
- 2)免疫調(diào)節(jié):抑制小膠質(zhì)細(xì)胞和T細(xì)胞的過度活化,減輕神經(jīng)炎癥;
- 3)抵抗損傷:幫助神經(jīng)元對抗興奮性毒性和氧化應(yīng)激,從而在動物模型中有效維持運(yùn)動功能。
臨床試驗(yàn)證實(shí)安全性,并顯示有限但具提示性的療效信號
早期I/II期臨床試驗(yàn)(通過鞘內(nèi)、靜脈或脊髓內(nèi)途徑)一致證實(shí)了MSC移植在ALS患者中的良好安全性和耐受性,未報(bào)告嚴(yán)重毒性或腫瘤形成。一些研究觀察到治療后肌萎縮側(cè)索硬化癥功能評定量表(ALSFRS)下降速度暫時(shí)減緩、肺功能穩(wěn)定等初步積極信號。
然而,一項(xiàng)針對基因工程改造的神經(jīng)營養(yǎng)因子遞送MSCs(MSC-NTF)的III期隨機(jī)對照試驗(yàn)未能達(dá)到主要療效終點(diǎn)。盡管次要終點(diǎn)(如腦脊液中炎癥和神經(jīng)營養(yǎng)標(biāo)志物的改善)和疾病較輕亞組的分析顯示了具有名義統(tǒng)計(jì)學(xué)意義的有限臨床改善,但這證實(shí)了其生物學(xué)活性,也表明目前的MSC療法在ALS中雖能帶來可測量的病理改善,但轉(zhuǎn)化為顯著臨床獲益的能力仍然有限,凸顯了進(jìn)一步優(yōu)化治療策略的必要性。
結(jié)論與未來方向
本綜述系統(tǒng)介紹了間充質(zhì)干細(xì)胞療法在阿爾茨海默病、帕金森病、亨廷頓病和肌萎縮側(cè)索硬化癥這四大神經(jīng)退行性疾病中的治療進(jìn)展。盡管在早期臨床試驗(yàn)中取得了顯著進(jìn)展,尤其是安全性得到初步驗(yàn)證,但后期關(guān)鍵試驗(yàn)的缺乏凸顯了進(jìn)一步深入研究的必要性。
新興策略正在積極應(yīng)對現(xiàn)有挑戰(zhàn):通過對MSCs進(jìn)行預(yù)處理、基因工程改造和生產(chǎn)工藝標(biāo)準(zhǔn)化,旨在提高其存活率、歸巢能力與分泌活性。同時(shí),對MSC來源的細(xì)胞外囊泡的興趣日益濃厚,它作為一種“無細(xì)胞”療法,保留了MSCs的旁分泌益處,并可能克服安全性、可擴(kuò)展性和遞送方面的限制。此外,日益重視生物標(biāo)志物指導(dǎo)的患者選擇和早期干預(yù),有助于未來試驗(yàn)更精準(zhǔn)地識別潛在獲益人群。
未來的研究應(yīng)致力于擴(kuò)大臨床試驗(yàn)的規(guī)模與病種范圍,并著力解決EVs生產(chǎn)的規(guī)模化與標(biāo)準(zhǔn)化問題。隨著對EVs療法興趣的增長、相關(guān)技術(shù)的進(jìn)步以及對其治療機(jī)制的深入理解,神經(jīng)退行性疾病的治療格局有望迎來革命性發(fā)展。這些進(jìn)展或?qū)⑼苿痈珳?zhǔn)、高效、微創(chuàng)的治療手段的誕生,最終改善神經(jīng)退行性疾病患者的臨床預(yù)后。
參考資料:
[1]:Trabulo, A.; Sousa, P.; Alvites, R.; Maurício, A. C. Mesenchymal Stem Cell-based Therapies Applied in Neurological Diseases. Preprints 2026, 2026010966. https://doi.org/10.20944/preprints202601.0966.v1
免責(zé)說明:本文僅用于傳播科普知識,分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時(shí)聯(lián)系我。




 掃碼添加官方微信
掃碼添加官方微信